 去看看
去看看


一、引言
围手术期经食管超声心动图(TEE)检查从形态和功能两个方面评估循环系统,具有定位、定性、定时、定量的基本功能,为围手术期诊疗决策提供依据,提高麻醉和手术的安全性和有效性。
围手术期合理应用标准化的超声心动图,可有效地监测循环事件,如:骨科和泌尿外科手术的肺动脉栓塞,开颅手术的气体栓塞,胸部创伤的心包压塞等。在超声循环监测方面常用于:血容量监测,整体和局部左心功能、右心功能评价,监测基本的瓣膜形态及功能变化,成人常见的先心病的形态和功能监测等。
超声心动图监测循环功能的思路是:通过对标准化切面的观察和测量,提取患者的心血管形态和功能特征,用病理生理学模型和循证医学证据解释,结合临床经验和诊疗规范用于诊疗决策。
本文针对围手术期TEE监测的一些关键问题,阐述如何采集并使用TEE图像来解决临床问题,重点介绍以诊疗决策为目的的超声循环监测方法,涵盖了国内外的最新进展。
二、TEE检查前评估
1.询问病史 心血管、肺专科病史,上消化道病史,糖尿病、高脂血症及高血压病史。
2.查体 心、肺专科体征,纽约心功能分级,口、咽部专科体征。
3.实验室检查 心肌酶、凝血功能、输血免疫全套。
4.评估病情 麻醉、外科操作引起术中血流动力学不稳定的风险。
5.是否需要行术中TEE检查,是否具备TEE检查的条件。
6.机械通气的重症患者行TEE检查需要随时关注通气情况。
三、TEE检查的适应证
1.术中出现难以解释的低血压、低血氧、低CO2分压,且难以纠正者。
2.血流动力学监测,观察前负荷、心肌收缩功能、心肌舒张功能、后负荷。
3.循环功能障碍,如休克类型的鉴别诊断。
4.心源性梗死诊疗决策所需的直接和间接征象。
5.急诊手术胸痛的鉴别诊断,如夹层动脉瘤、肺栓塞、心肌梗死的鉴别。
6.创伤急诊手术麻醉,需要排除心脏和大血管的并发症,如心脏破裂、主动脉横断等。
7.心脏瓣膜功能检查。
8.经胸超声检查显像困难,难以明确各种心脏大血管形态和功能异常。
四、TEE检查的禁忌证
1.绝对禁忌证:患者拒绝、活动性上消化道出血、食管梗阻或狭窄、食管占位性病变、食管撕裂和穿孔、食管憩室、食管裂孔疝、先天性食管畸形、食管手术后不久。
2.相对禁忌证:食管静脉曲张、凝血障碍、纵隔放疗史、颈椎疾病、咽部脓肿、咽部占位性病变。相对禁忌证需要比较TEE检查的收益和相对禁忌证的风险决定是否行TEE监测。
五、患者的准备
1.签署同意书。
2.全麻状态下可选择仰卧位和侧卧位。
3.检查并清除患者口腔内和食管内活动性异物。
4.气管导管固定于患者嘴角一侧,便于探头置入。
5.放置探头前胃管负压吸引,以获得清晰的TEE图像。
6.TEE探头放置后5分钟,检查无活动性出血,再放置鼻咽部温度探头。
7.围手术期TEE检查时,注意不要影响患者的通气。
8.清醒的患者可行口咽部局部麻醉,在侧卧位下置入探头。
9.除超声心动监测外,还要密切观察心电图波形、有创动脉波形、无创血压、血氧饱和度、呼末CO2等监测指标,以便及时发现和处理异常状况。
六、TEE探头的安全使用
1.检查探头结构是否正常,将探头与超声主机妥善联接,在控制面板上找到探头驱动软件,选择所需检查模式。
2.消毒的探头前端换能器面涂上超声耦合剂。
3.右手持探头管体前1/3处,左手中指、食指和大拇指轻提下颌,打开咽腔、轻柔地将探头送至咽后壁,如遇到阻力,稍前屈探头,通过咽后壁阻力点后,将探头稍向右旋转,用探头细心体会食管开口的位置,观察颈部两侧与梨状窝对应部位,使用恰当的手法,尽量轻柔地将TEE探头推送过食管开口。
4.TEE探头置入困难时禁用暴力,必要时使用喉镜、可视喉镜辅助,或者寻求他人帮助。尝试3次以上未能成功置入探头,或者在放置过程中发现活动性出血,应考虑放弃使用TEE检查。
5.成人TEE探头建议最低安全体重为30kg,儿童TEE探头要求最低安全体重为5kg,新生儿TEE探头用于体重低于5kg的患儿。
6.在TEE检查过程中要注意检查口咽部有无出血,及时发现和处理相关并发症。
7.退出探头时遇到阻力,需要确认探头是否处于前端弯曲状态并被卡锁固定,先解除卡锁,将探头轻柔送入胃内,调直探头后方可重新退出,全麻患者各种保护反射受到抑制,应尽量保护患者。
8.对血液传播性疾病的患者必须用透声性能良好的探头套隔离TEE探头。
七、TEE检查的操控及术语
TEE图像总的原则是:探头接触患者的位置是图像的顶点,改变探头的位置就是改变TEE图像在人体空间内的位置。TEE探头呈长管状,探头运动受消化道的限制,整体运动只有8种,分别是:推进、后退;左转、右转;前屈、后屈;左屈、右屈(图6-1)。
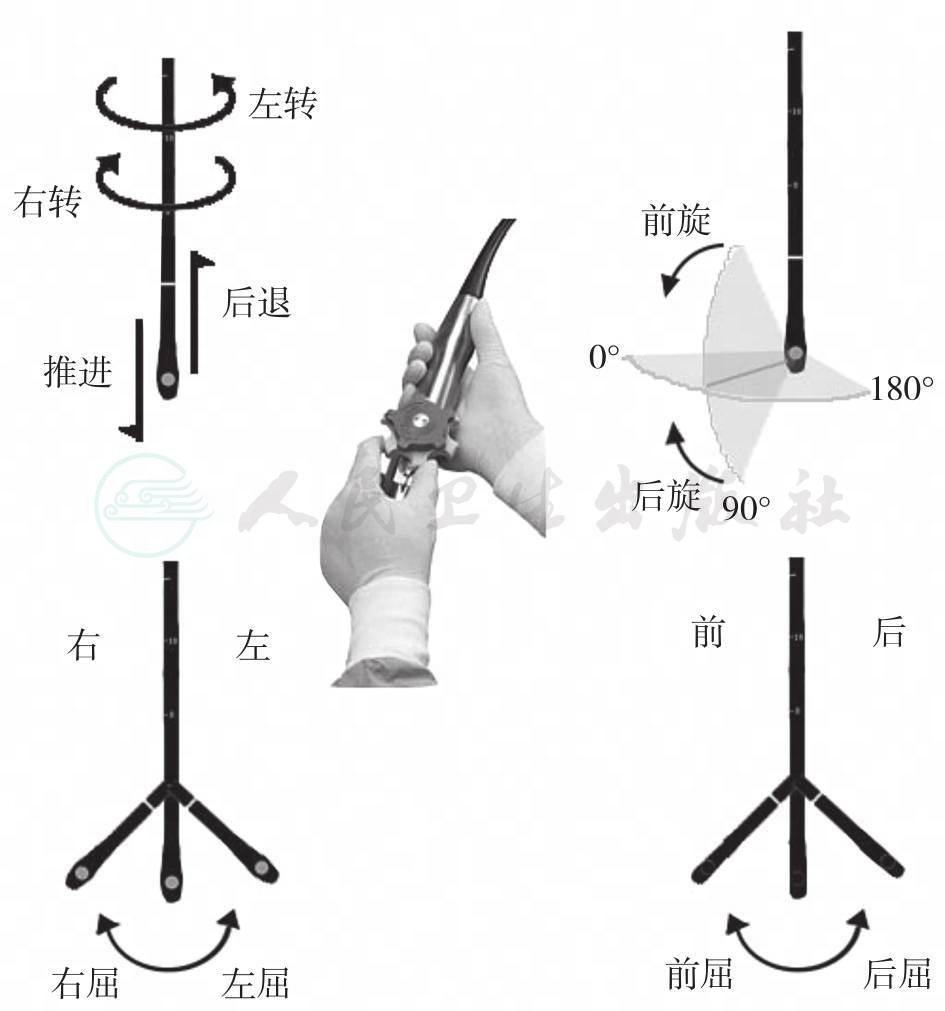
图6-1 TEE探头的8种运动及操控示意图
1.手握TEE探头向食管远端或胃推进称“推进”,反之为“后退”。手握探头朝向患者右侧转动称之为“右转”,逆时针转动称之为“左转”。
2.使用操作柄的大轮将探头前端向前弯曲称之为“前屈”,向后弯曲称为“后屈”。使用操作柄的小轮将探头顶端向左方弯曲称之为“左屈”,反之称为“右屈”。
3.TEE探头处于某一个姿态不动时,在探头保持静止的状态下,可通过手柄上的2个圆形按键,调节声平面角度从0°~180°,称为“前旋”,反向调节声平面角度从180°~0°,称之为“后旋”。
八、TEE图像的方位和视角
超声主机屏幕和出版物的TEE图像通常被默认属于室内空间,室内空间的方位和坐标和人体空间不同,造成切面、心脏模型和人体空间之间的联系难以理解和交流,因此,TEE图像应该遵循二维或三维切面解剖学的原则,将TEE图像还原到患者的解剖空间,统一人体模型、心脏模型和超声切面。
2D或是3D图像(图6-2)都需要定义视角,采取面对心脏模型的视角,有2个理由:①面对心脏模型与系统解剖学方位一致,便于沟通;②面对心脏模型有利于实现从TEE到TTE的快速切换。以食管中段4腔心切面为例,描述探头与图像的位置关系理解图像和心脏模型的位置关系(图6-3),直观地显示了探头、切面与心脏模型的空间关系。
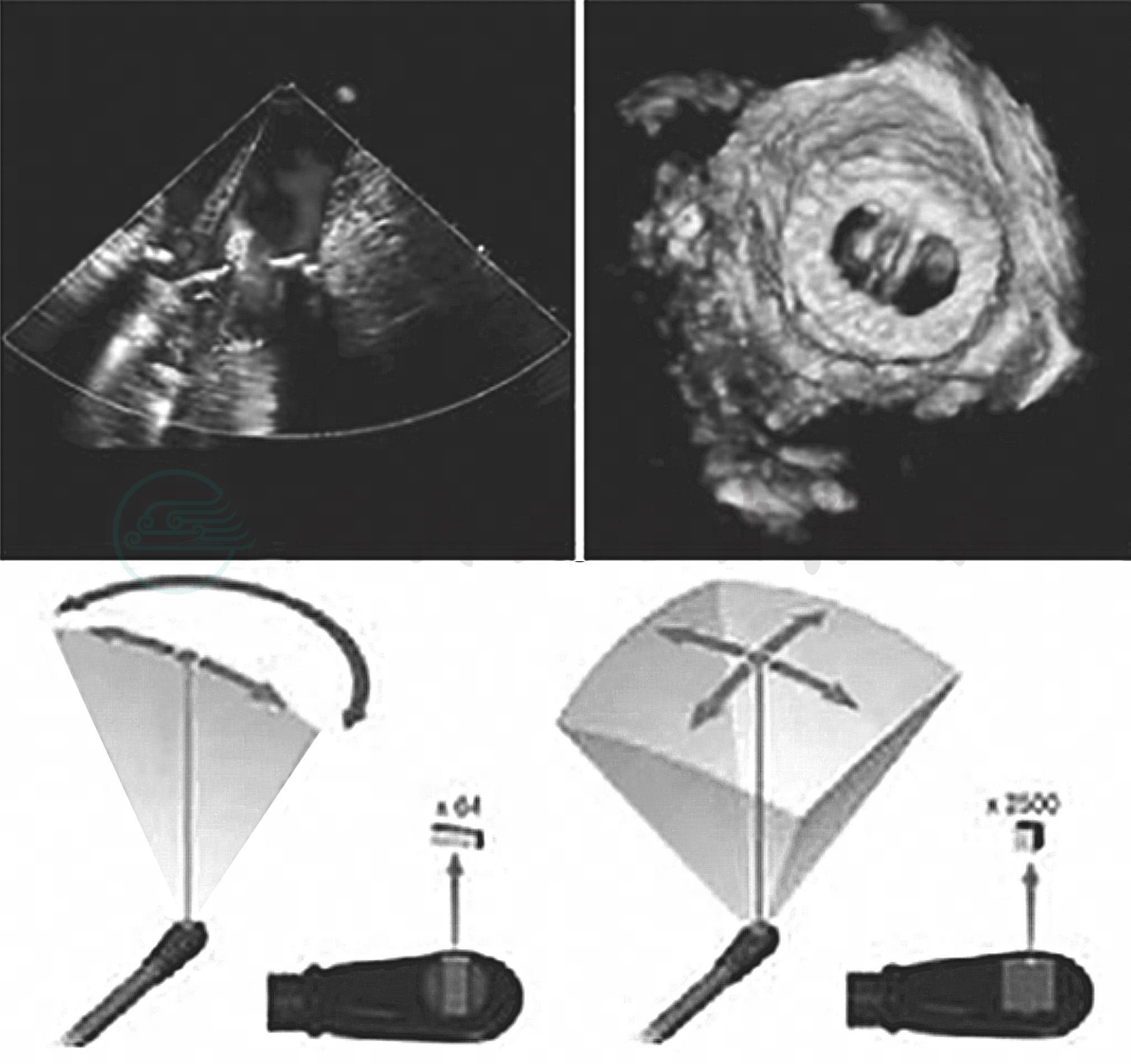
图6-2 2D和3D图像及成像原理图
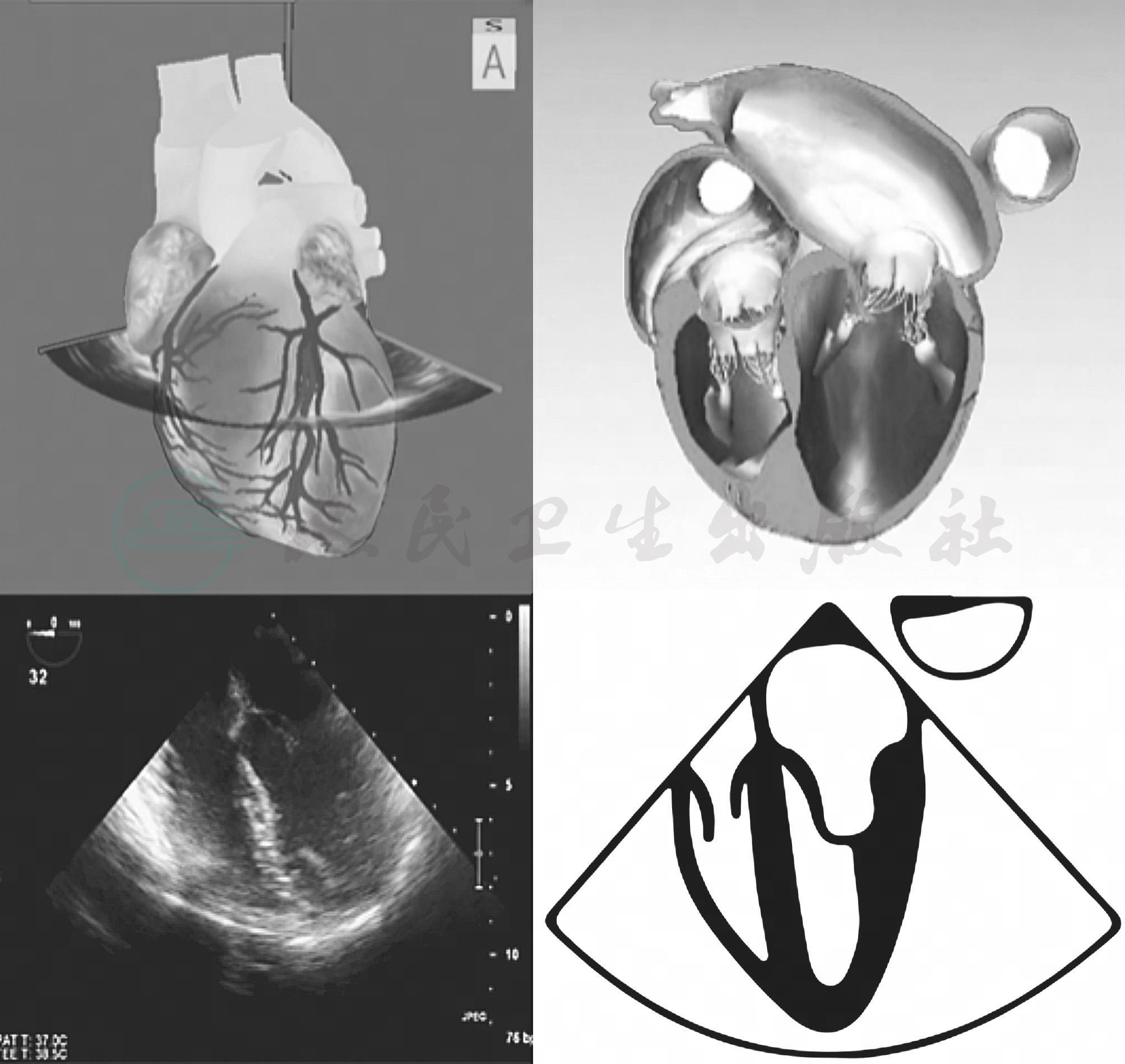
图6-3 食管中段4腔心切面及模型图
九、TEE检查切面的标准化
围手术期的工作特点决定了TEE检查切面必须标准化,自TEE进入临床,切面标准化工作就没有中断过。1996年美国麻醉医师协会(ASA)和美国超声心动图学会(ASE)一起确立了术中TEE监测的20个标准切面,对全世界术中TEE推广培训具有里程碑意义。随后,ASA和ASE每隔3~4年不断更新和增减内容,2013年美国心血管麻醉医师协会和美国心脏超声协会共同发表联合声明,将20个TEE标准切面简化到11个(图6-4)。在这份专家共识中我们重点介绍20个标准切面和中国的TEE-Focus 6个基本切面的采集和临床应用。
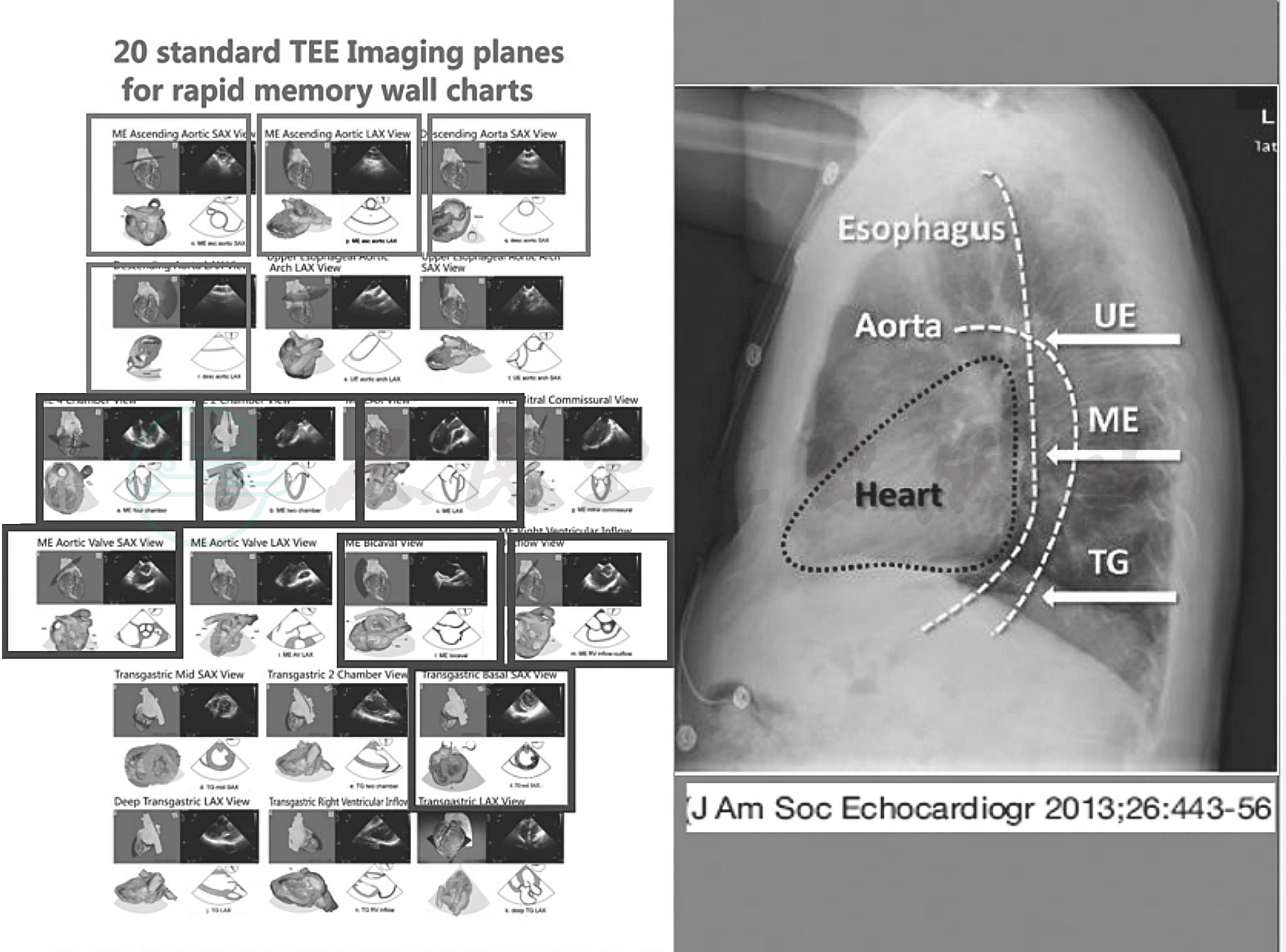
图6-4 11个标准切面示意图
1.20个TEE检查标准切面(表6-1)
2.11个标准平面介绍
2013年美国心血管麻醉与心血管超声联合声明推荐的11个标准切面,相比TEE20个标准切面,最显著的特点是:6个经胃切面,只保留了中段左心室短轴切面,说明该切面在围手术期具有重要的监测价值;6个大血管切面去掉了2个切面:食管上段主动脉弓长轴和短轴切面;8个食管中段切面去掉了2个切面:主动脉瓣长轴切面和二尖瓣交界切面(图6-3)。
3.TEE-Focus 6个基本平面
2013年中国麻醉医师术中TEE推广培训协作组提出了适用于麻醉急诊和术中循环监测的TEE-Focus的概念,其基本切面有5个,临床实践证明适用于术中循环的监测。本专家共识建议增加升主动脉长轴切面,因为动脉粥样硬化斑块形成的患者数量在增加,此处有无粥样斑块及斑块的分级对体外循环手术主动脉插管的安全性监测很重要。
截至目前,TEE-Focus包含6个基本切面(图6-5,图6-6,表6-1),其中有4个关于心脏的基本切面和2个关于大血管的基本切面:①左心室长轴切面,②右心室流入流出道切面,③经胃底心室短轴切面,④食管中段4腔心切面,⑤降主动脉短轴切面,⑥升主动脉长轴切面(新增)。
十、 TEE-Focus观察与测量的基本内容
围手术期TEE检查时间有限,需要迅速决断,往往来不及做精确的测量,所以我们首先应该明确要观察什么,其次是怎么测量的问题,要获得可靠的决策依据必须对标准化切面进行有效的观察与测量。
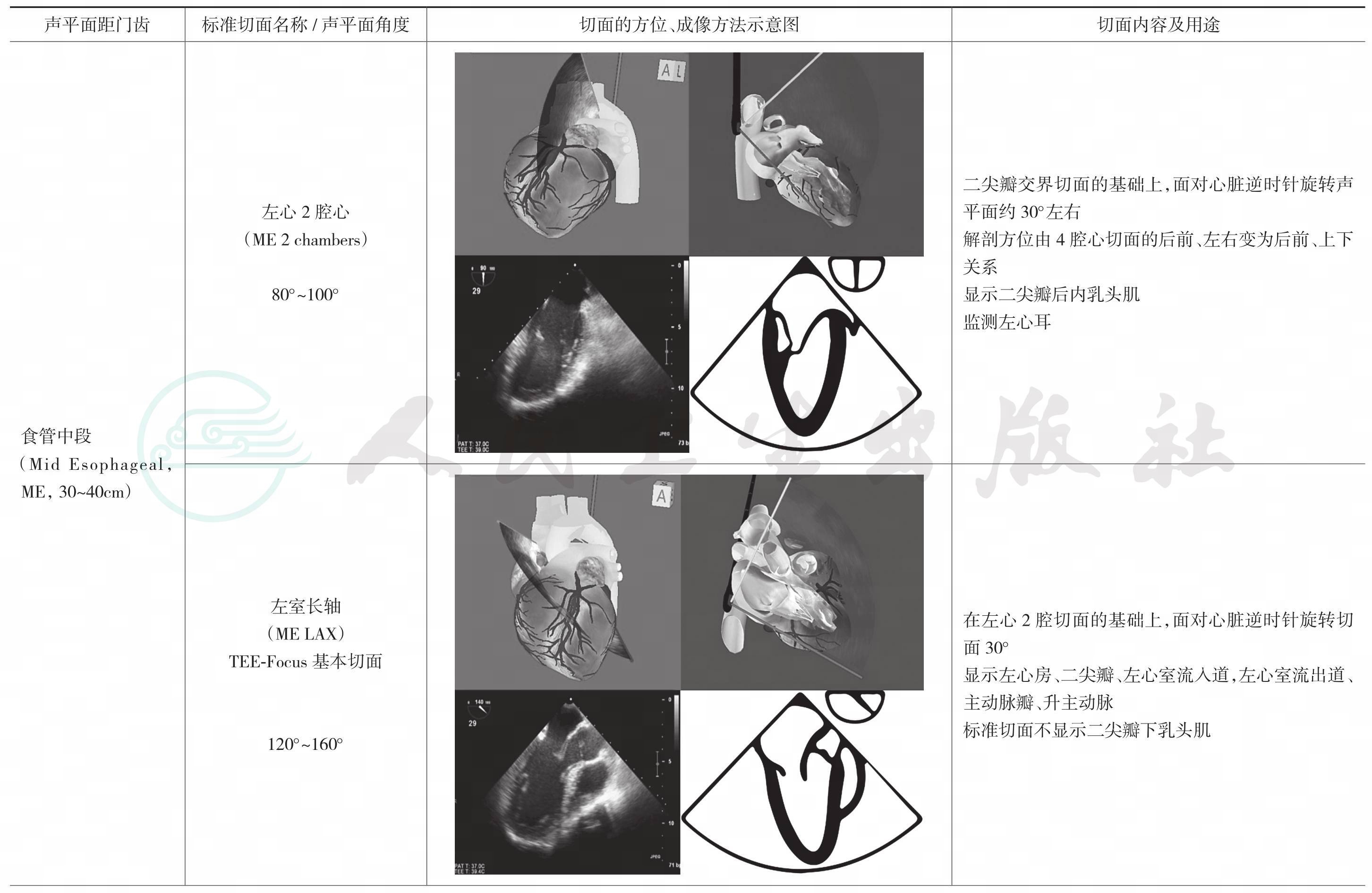
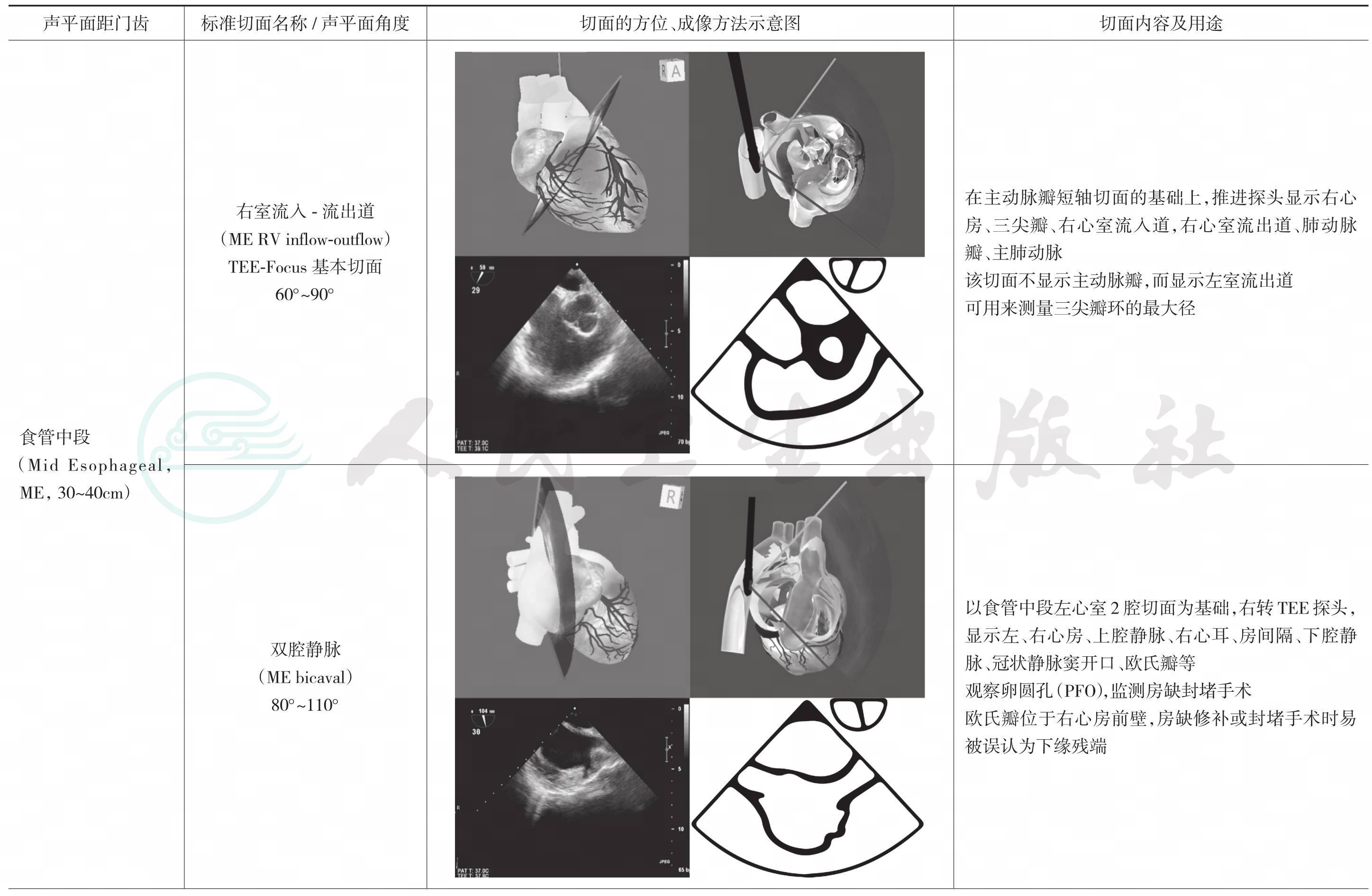
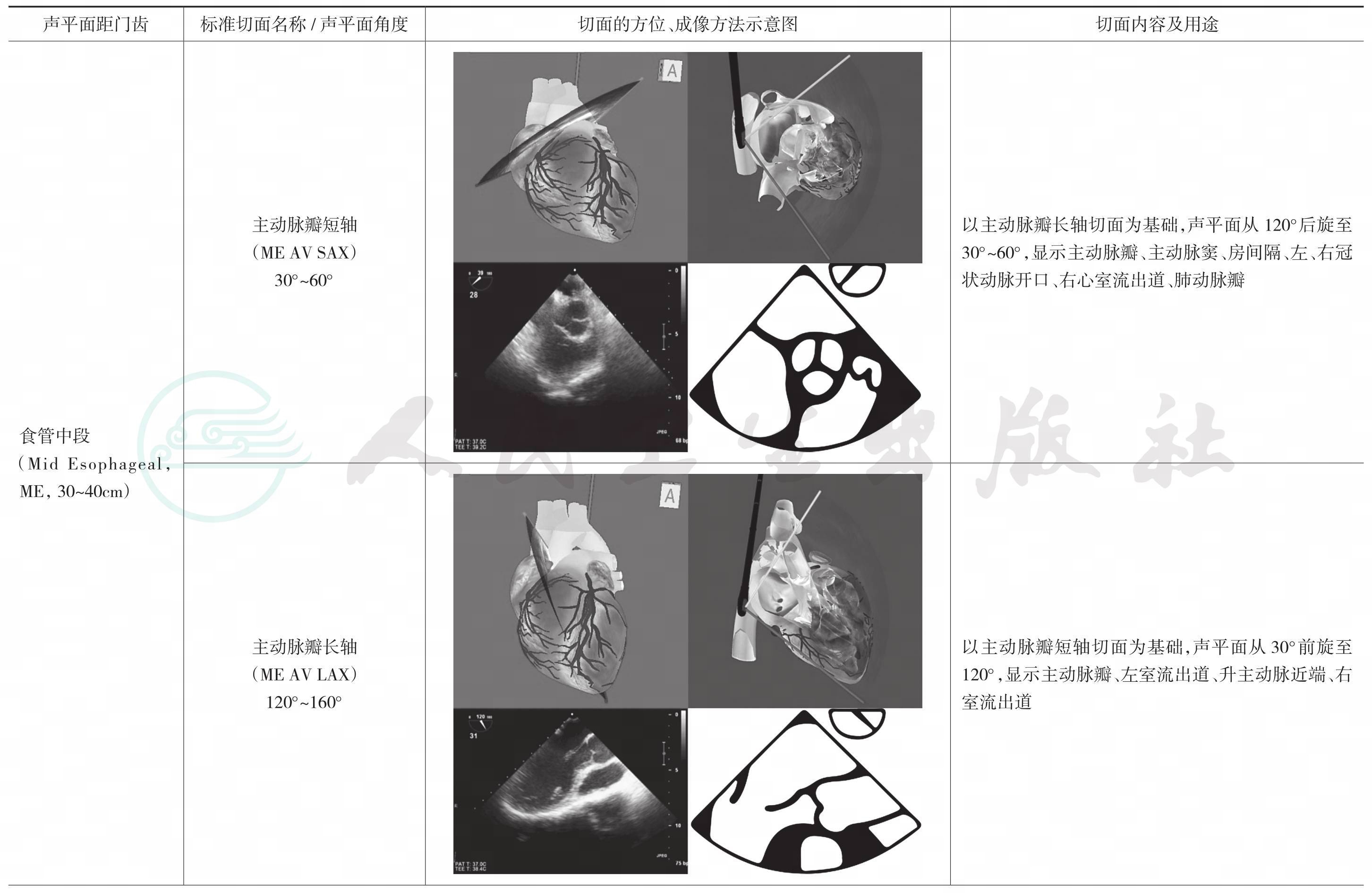
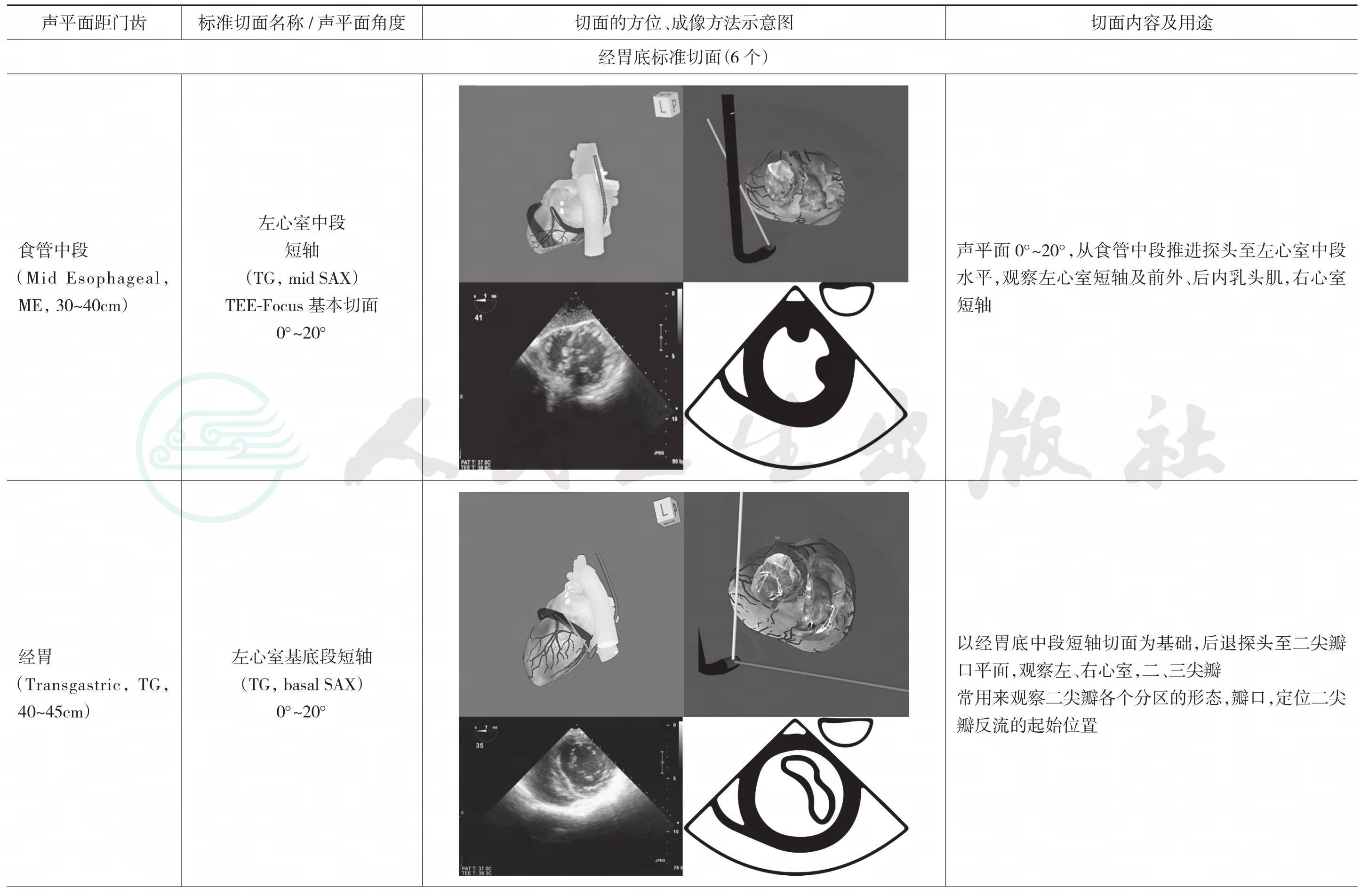
表6-1 20个TEE检查标准切面一览表(含6个Focus-TEE基本切面)
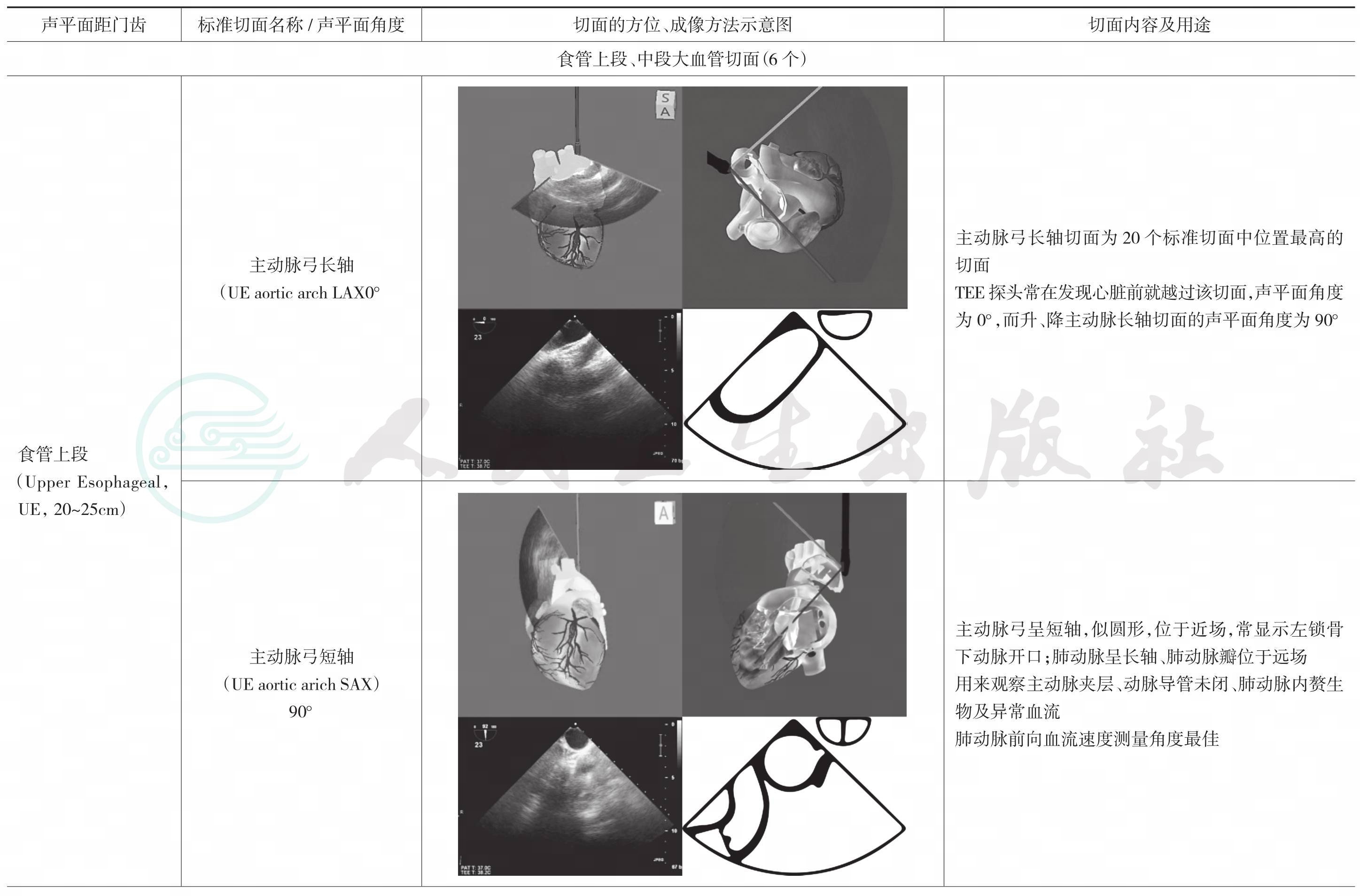
续表
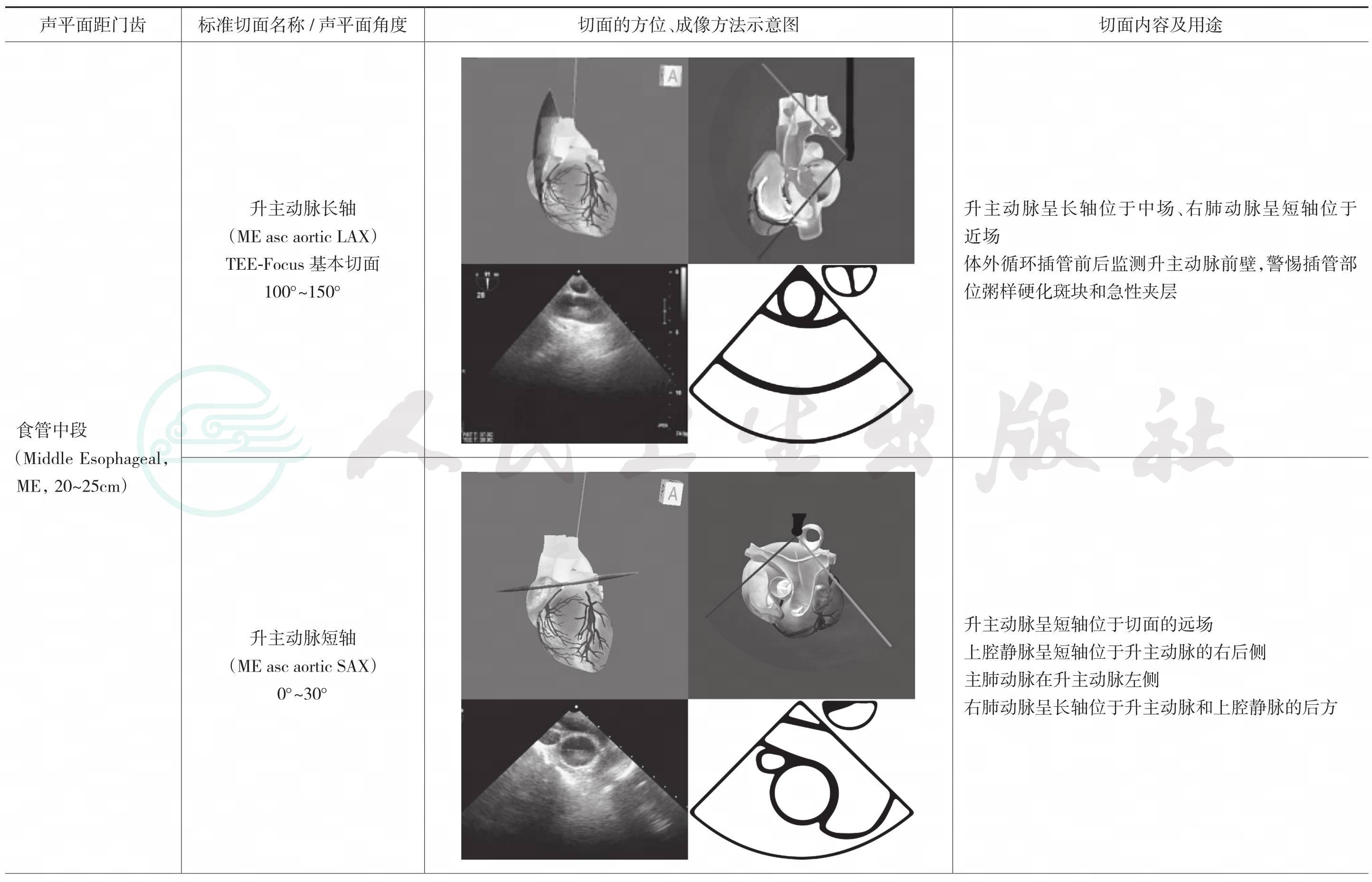
续表
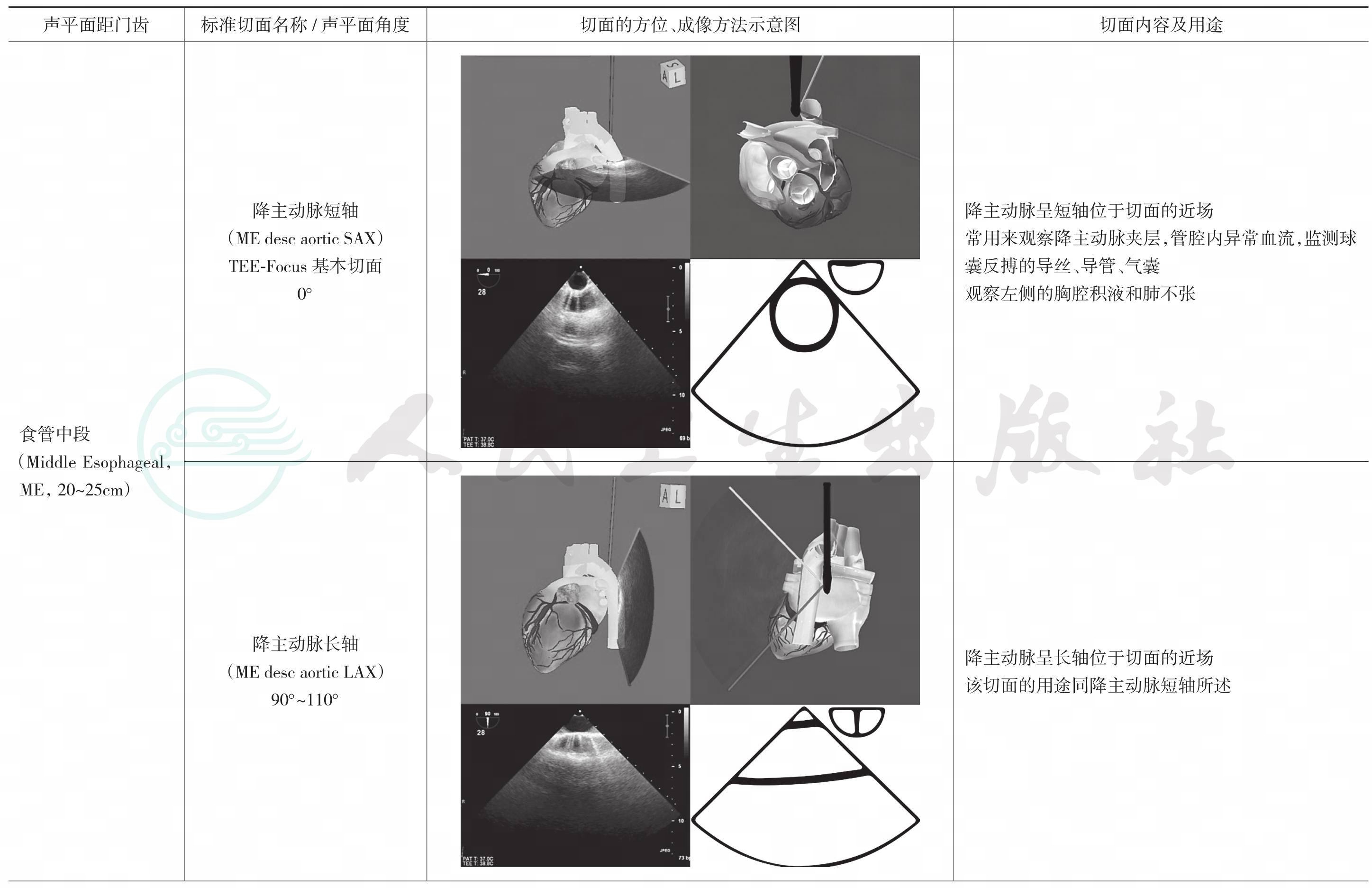
续表
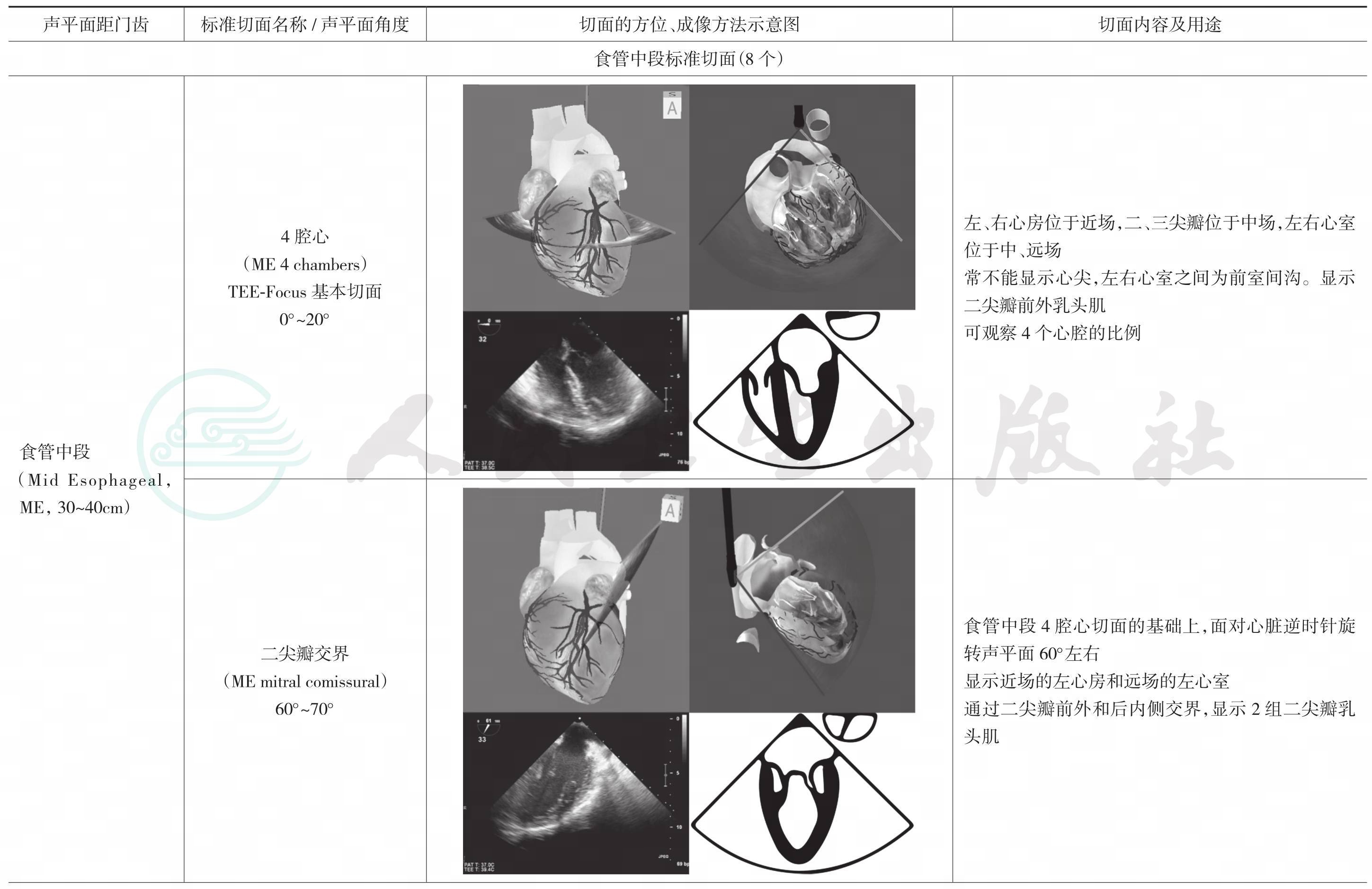
续表
续表
续表
续表
续表
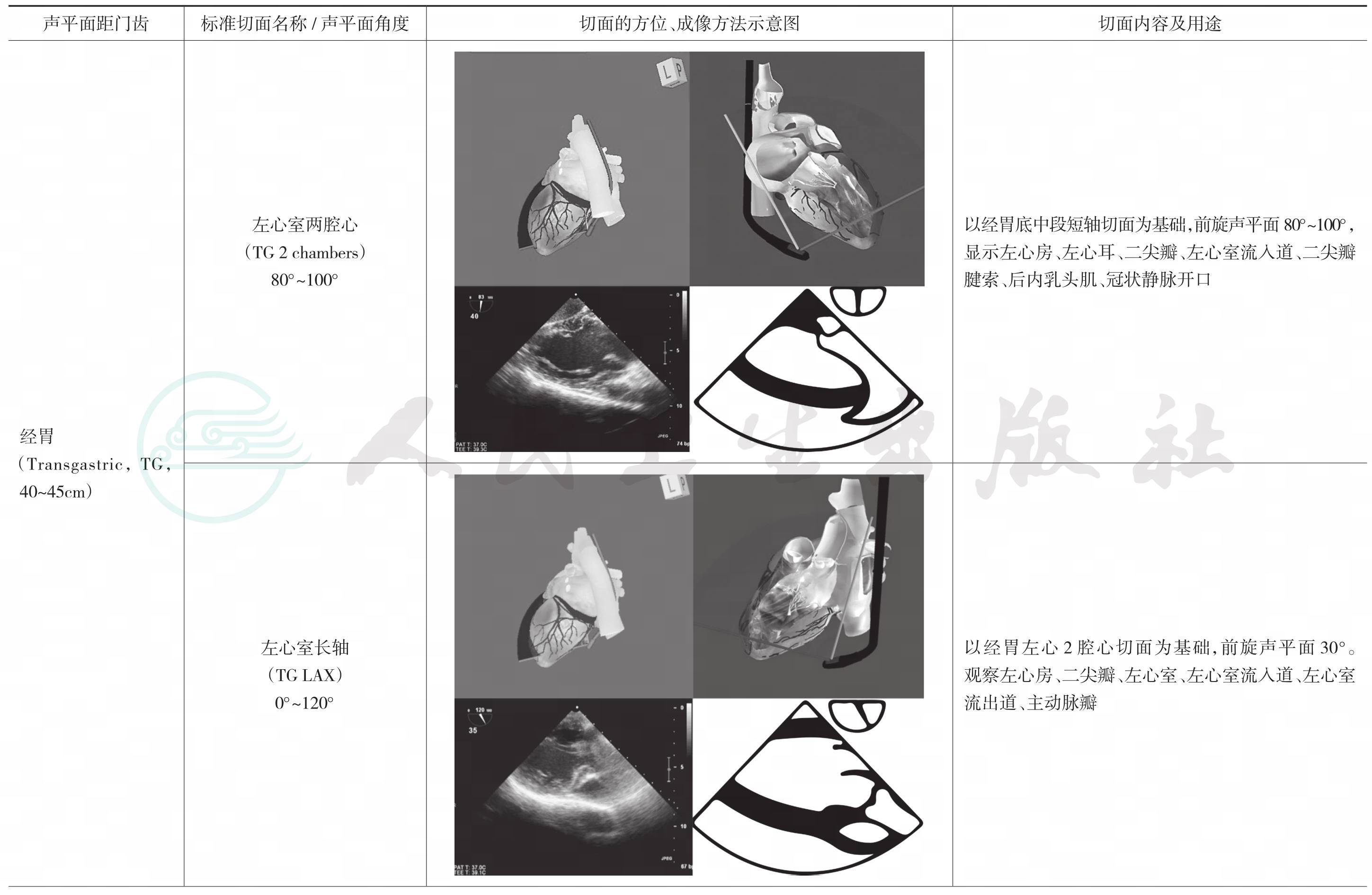
续表
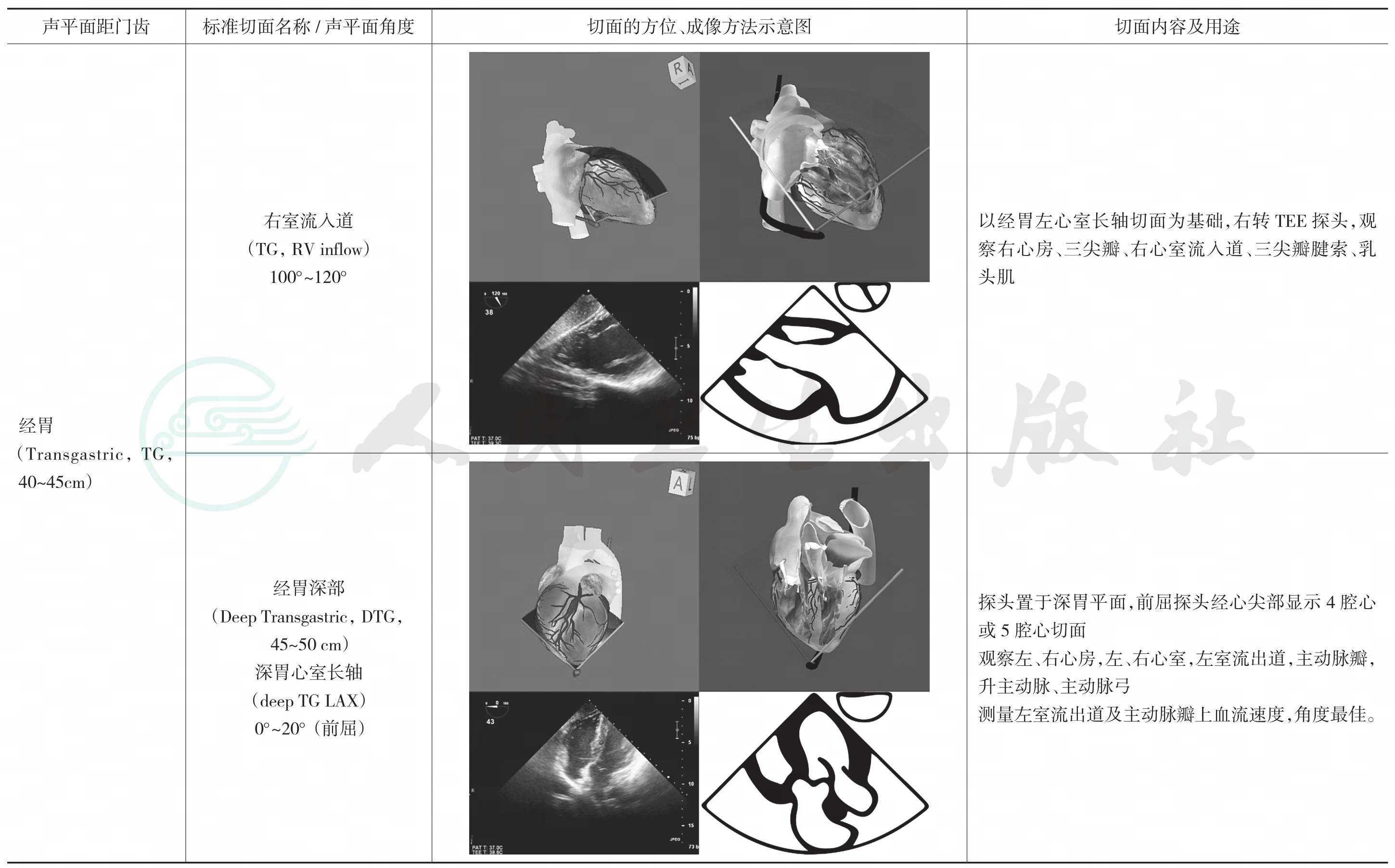
常用缩略语:UE,食管上段;ME,食管中段;TG,经胃; LAX,长轴;SAX,短轴;Asc,升主动脉;AV,主动脉瓣;CS,冠状静脉窦;desc,降主动脉;IAS,房间隔;IVC,下腔静脉;LA,左心房;LAA,左心耳;LV,左心室;LVOT,左心室流出道;MV,二尖瓣;PA,肺动脉;prox,近端;PV,肺动脉瓣;RA,右心房;RV,右心室;RVOT,右心室流出道;SVC,上腔静脉;TV,三尖瓣
TEE-Focus 将TEE检查的核心观察内容概括为:壁、腔、瓣、流四个方面(表6-2),壁就是房壁、室壁、血管壁,腔就是心房、心室腔和血管腔,瓣就是房、室之间的两个房室瓣、心室和大动脉之间的两个半月瓣,流就是心血管的正常和各种异常血流,其中壁和瓣是心血管系统的固体成分,腔和流是心血管系统的液体成分,循环系统特殊的液体和固体的耦合派生出了各种血流动力学参数。
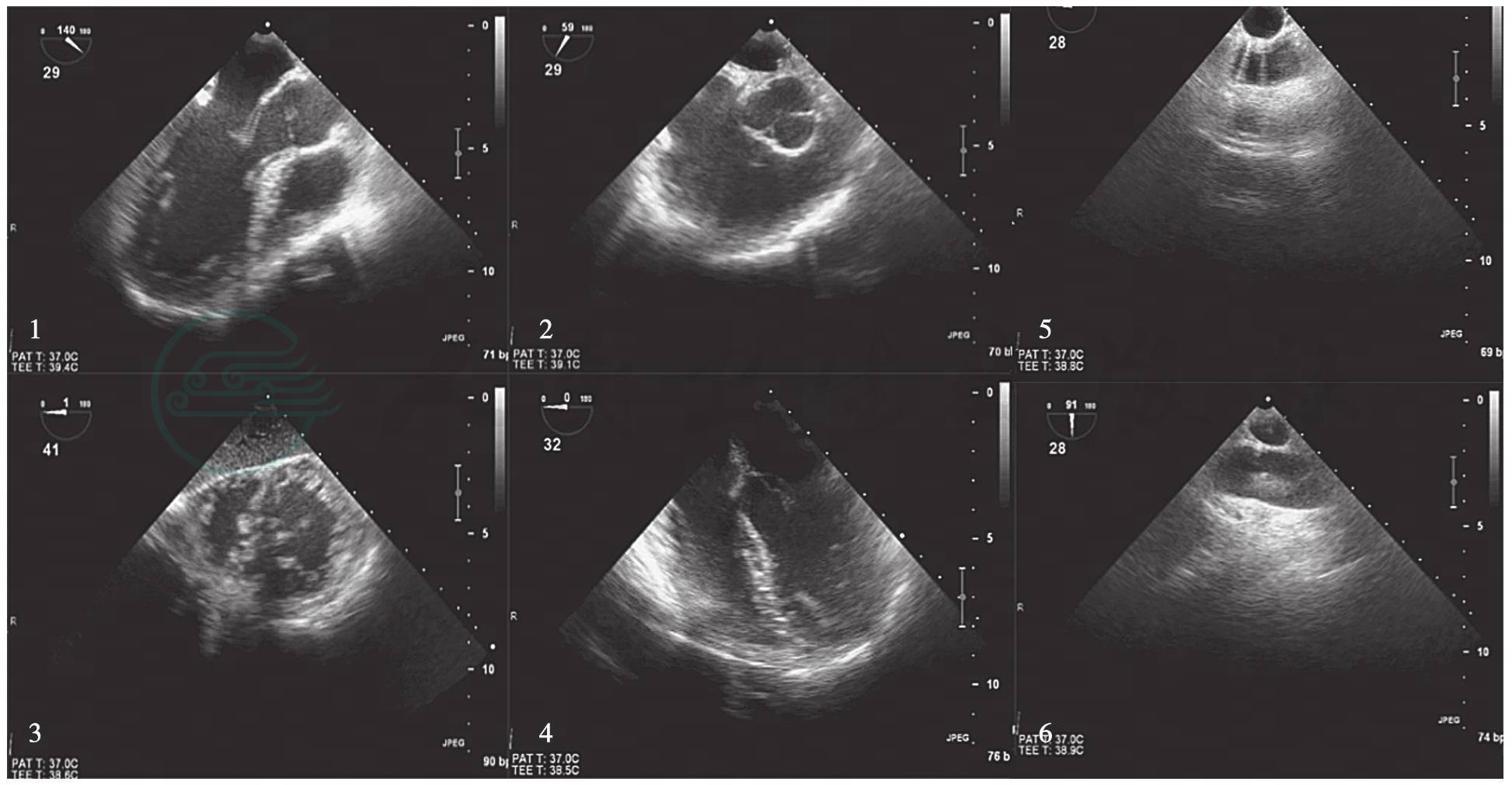
图6-5 TEE-Focus 6个基本切面的2D图像
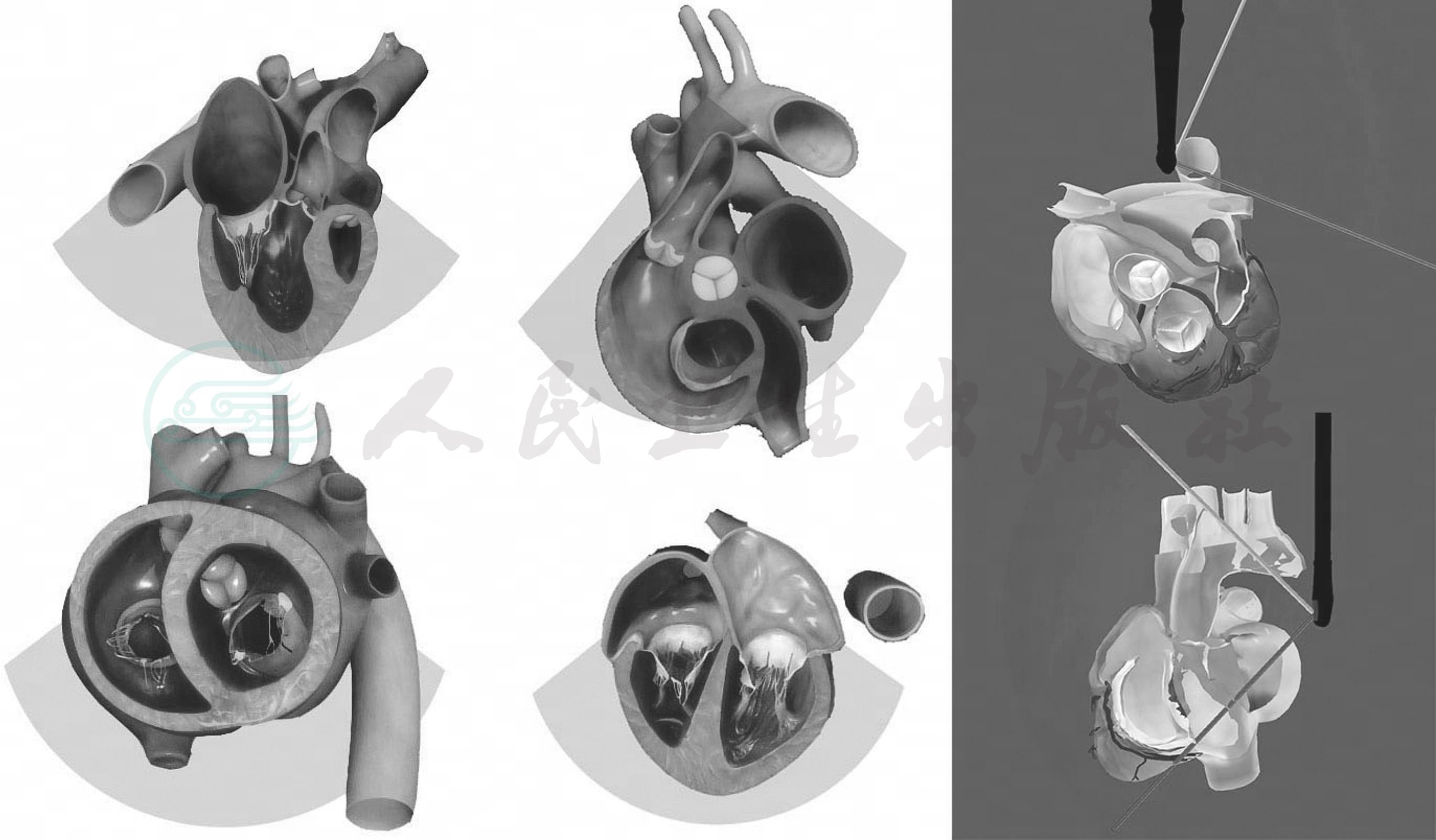
图6-6 TEE-Focus中的6个基本切面的模型切面
1.左心室长轴切面
①左心房大小、房壁厚度是否正常,舒缩运动是否正常;②二尖瓣开闭运动是否正常,有无穿孔及赘生物;③左心室流入道是否通畅;④左心室,室壁厚度是否正常,舒缩运动是否正常;⑤左心室流出道是否有梗阻;⑥主动脉瓣开闭是否正常,有无赘生物;⑦升主动脉管壁、管腔是否正常;⑧腔内血流是否正常。
2.右心室流入流出道切面
①右心房大小、房壁厚度是否正常,舒缩运动是否正常;②三尖瓣开闭运动是否正常,有无穿孔及赘生物;③右心室流入道是否通畅;④右心室大小,室壁厚度是否正常,舒缩运动是否正常;⑤右心室流出道是否有梗阻;⑥肺动脉瓣开闭是否正常,有无赘生物;⑦肺动脉管壁、管腔是否正常;⑧腔内血流是否正常。
表6-2 TEE-FOCUS标准切面的观察内容

3.经胃左心室短轴切面
①左、右心室腔大小及形态;②左、右心室比例及室间隔凸向哪一侧;③室壁厚度和搏动幅度;④腔内血流是否正常。
4.食管中段四腔心切面
①各房室大小及其比例;②切面中心室壁的厚度、搏动幅度、连续性;③二尖瓣和三尖瓣的形态结构和开闭功能;④腔内血流是否正常。
5.降主动脉短轴切面
①降主动脉管腔大小及形态;②主动脉壁各层是否增厚,回声增强;③是否存在夹层或假性动脉瘤;④腔内血流是否正常。
6.升主动脉长轴切面
①升主动脉管腔大小及形态;②主动脉壁各层是否增厚,回声增强,是否存在附壁血栓和粥样斑块;③是否存在夹层或假性动脉瘤;④腔内血流是否正常。
十一、TEE标准化切面的参数测量
1.心血管壁、腔参数测量参考值
正常值是描述正常心脏结构和功能的基础,最重要的参数莫过于心血管腔的内径和房室、血管壁的厚度。通过将测量值与正常参考值(表6-3)的比较,即可发现心血管的影像学异常。
2.左心室参数测量及功能评价
定性分析后可以对左心室功能进行进一步的定量评价。所谓定性分析,是在观察了一系列前述的正交切面后对左心室射血分数做出的目测评价。TEE的左心室定量分析,可以比照TTE的M型、二维和多普勒方法,但是还缺乏TEE的正常值。
表6-3 心血管壁、腔超声测量正常参考值
左心室有两条功能曲线,容积-时间曲线(图6-7)和压力-时间曲线,左心室容积-时间曲线的最大值点对应着左心室舒张末容积,最小值点对应着左心室收缩末容积,最大值点和最小值点之间的差值反映每搏输出量(SV)。EF(射血分数) =SV/EDV。
术中获得实时精确的LV容积-时间曲线尚不容易,需要用实时三维超声心动图技术、二维和三维图像自动分割技术(图6-8)、结合辛普森法计算得到,这种方法用在术中监测左心室的容积-时间曲线成本较高。如果心室形态正常,我们还是推荐用M型超声测量LVEDD/LVESD,计算FS(FS=LVEDD-LVESD/LVEDD)或者左心室中段短轴2D切面测量计算FAC=LVEDA-LVESA/ LVEDA;EF≈2FS。
3.左心室舒张功能
TEE可以准确而有效地评价左心室舒张功能,包括二尖瓣口血流、肺静脉血流和组织多普勒频谱的测量。较TTE,TEE在这些测量中的优势是能获得更好的多普勒取样线角度。如果TTE图像质量差或者探头无法在胸前放置,则可以改用TEE方法评价左心室舒张功能。有研究报道,对于进行冠状动脉搭桥手术的患者,仅应用二尖瓣环侧壁位点的e’峰≤10cm/s和跨二尖瓣的E/e’≤8就可以简单地评价左室舒张功能障碍,并预测远期主要心血管事件的发生。
4.经胃底左心室短轴切面评价心功能
以左心室中段短轴切面为例(图6-9),在这个切面上,可以观察左、右心室的心腔大小,室壁厚度。左心室内经正常值男性55mm,女性50mm,正常情况下左心室和右心室横径的比例关系大约是5:2;而左心室舒张末面积(LVEDA)和左心室收缩末面积(LVESA)的比例大致是2:1。

图6-7 左心室短轴切面与左心室容积/面积-时间曲线的关系
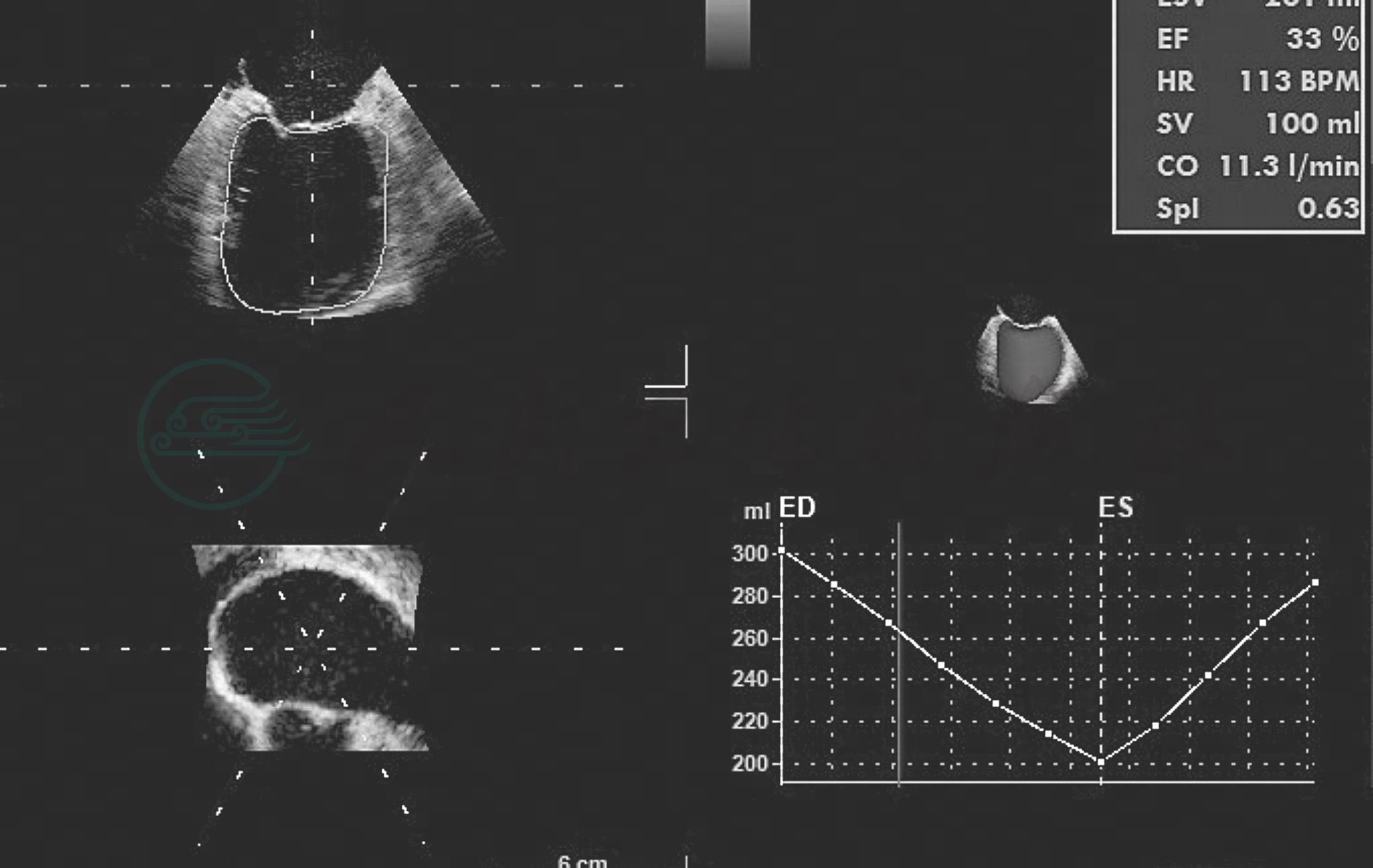
图6-8 3D-TEE 获得左心室容积-时间曲线
TEE-Focus左心室舒缩异常的超声图像监测模式(图6-9,表6-4):
(1)外周血管扩张模式(图6-9A)的特征是左房压正常,LVEDA正常,LVESA显著减小,差值增大,比值增大,室壁运动正常/增强;
(2)心衰模式(图6-9B)的特征是左房压升高,LVESA与LVEDA均增大,差值减小,比值减小,室壁运动减低;
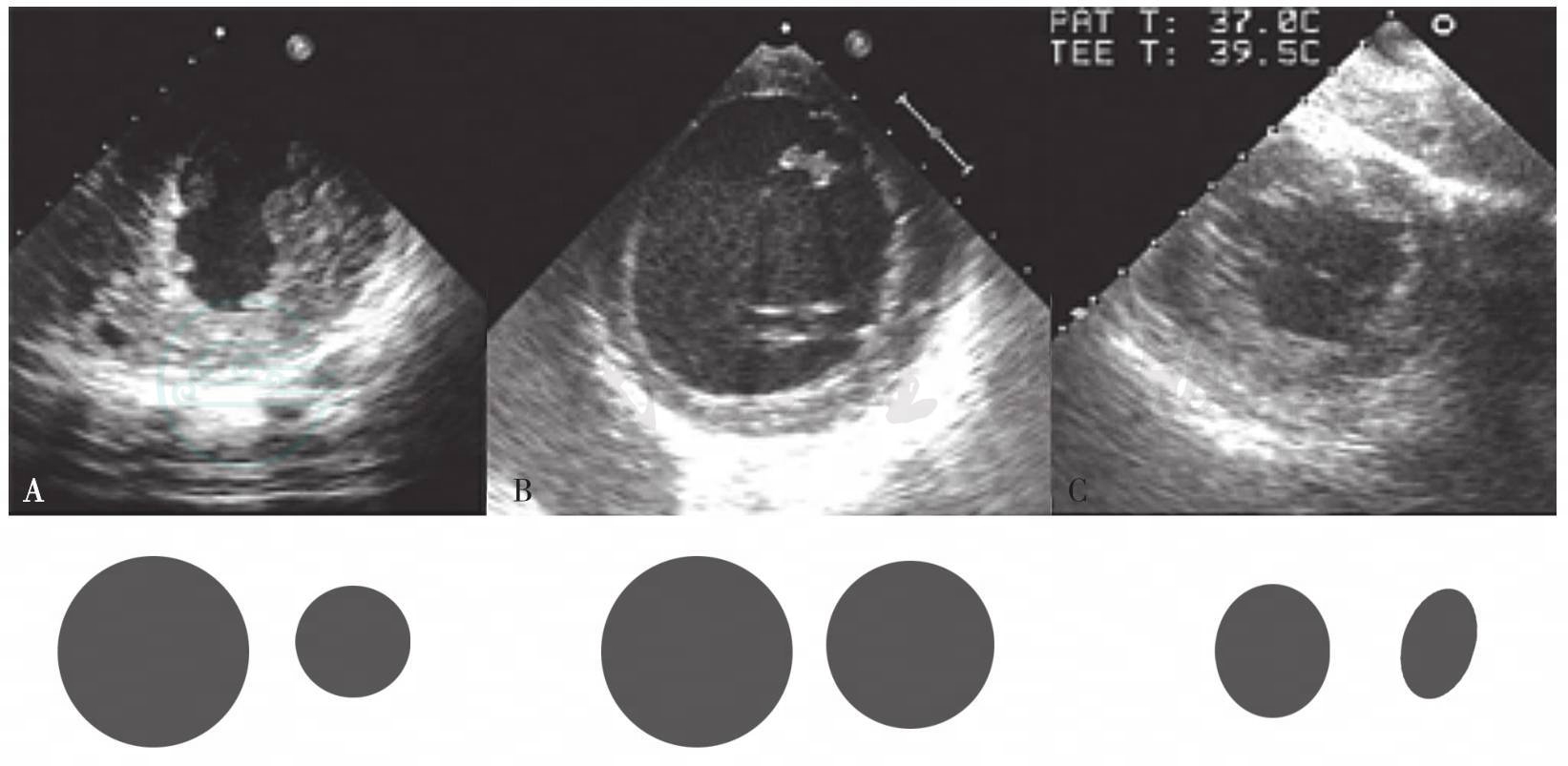
图6-9 经胃底左心室短轴切面用于心功能判断
(3)容量不足模式(图6-8C)的特征是左心房压降低,LVESA与LVEDA均减小,差值减小,比值减小,室壁运动正常/增强。
表6-4 经胃底左心室短轴切面用于左心室功能评价

5.二尖瓣参数测量及功能评价
二尖瓣是左心房和左心室之间的血流阀门,二尖瓣的开闭依靠房、室压差的驱动。二尖瓣环是具有动态变化性能的纤维肌性环,呈马鞍形,收缩期瓣环径缩小,朝向心尖运动,舒张期瓣环径扩大,背离心尖运动。二尖瓣有两个瓣叶,前叶约占二尖瓣表面积的三分之二,后叶呈C型,盘绕在前叶周围,占二尖瓣周长约三分之一,二者在前外侧和后内侧交界处会合。二尖瓣的前、后叶均可分为三个小叶,二尖瓣瓣叶左心室面的腱索附着在两组乳头肌上,分别为前外侧乳头肌和后内侧乳头肌。每一组乳头肌发出腱索附着在相邻的前后瓣叶上。
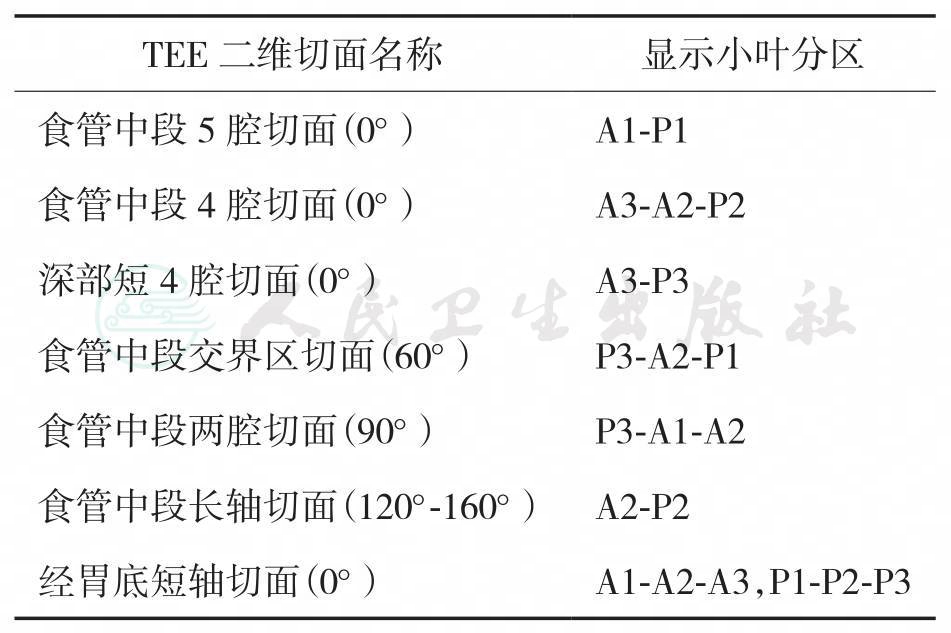
TEE切面可用来评估二尖瓣系统的每一部分,检查时将探头送至食管中段,操纵探头调整成像的角度使声平面对准二尖瓣环中心,探头晶片置于0°~10°食管中段4腔心切面后开始旋转声平面,依次获得食管中段二尖瓣交界切面、食管中段左心室2腔切面、食管中段左心室长轴切面,在各个标准切面上可以观察不同小叶的功能状态,各个小叶与标准切面的对应关系如图6-10所示。
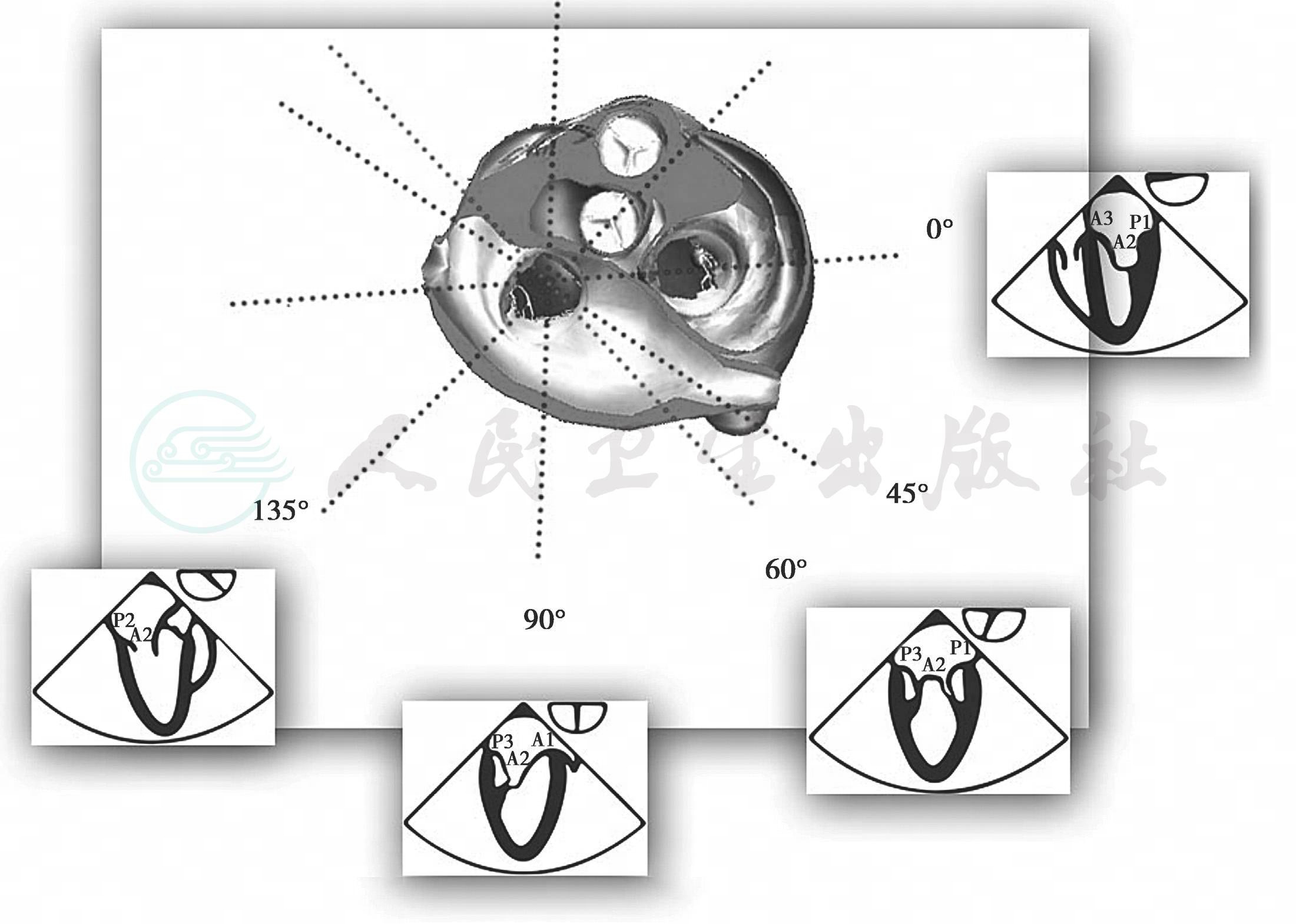
图6-10 TEE评价二尖瓣形态和功能的基本切面(标注二尖瓣分区)
TEE切面与二尖瓣分区的对应关系可用于二尖瓣脱垂部位的判断,但要注意的是:一定要将2D或3D图像与二尖瓣模型对应起来,不理解切面和模型之间的空间关系,直接用文献上的分区对应实际的超声图像会导致定位不准和交流障碍(图6-11~图6-14);另外,经胃底基底段短轴切面对诊断瓣叶裂和穿孔很有帮助,彩色多普勒可以提供有关反流束起源的信息(图6-14)。
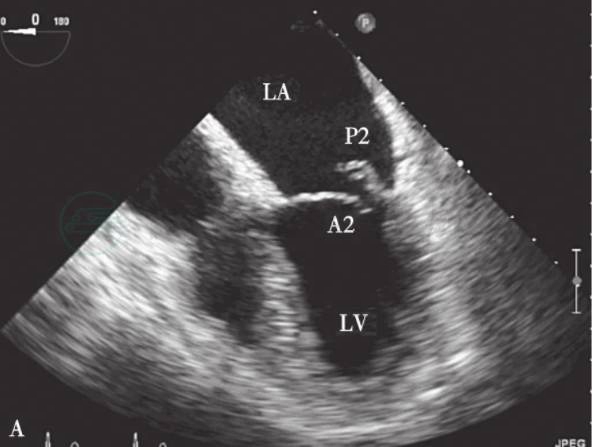
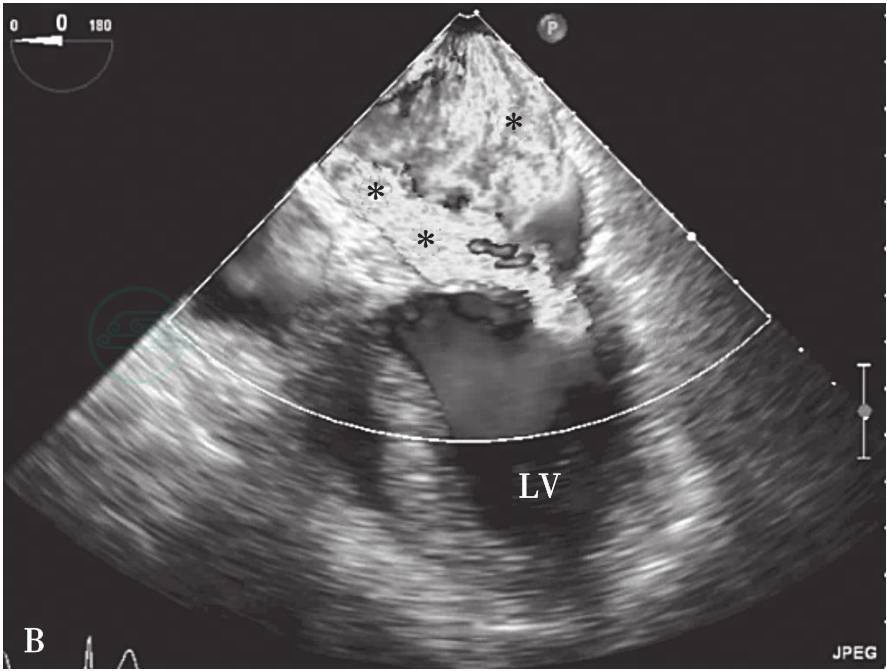
图6-11 四腔心切面显示二尖瓣后叶P2区脱垂
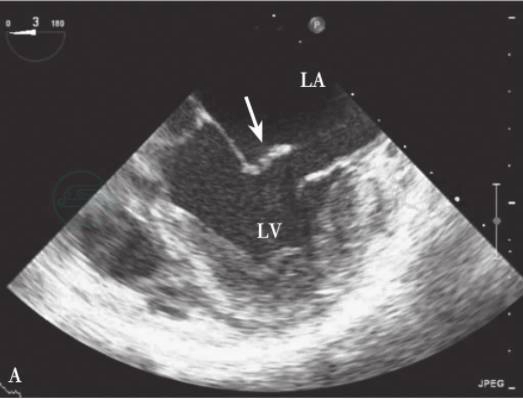
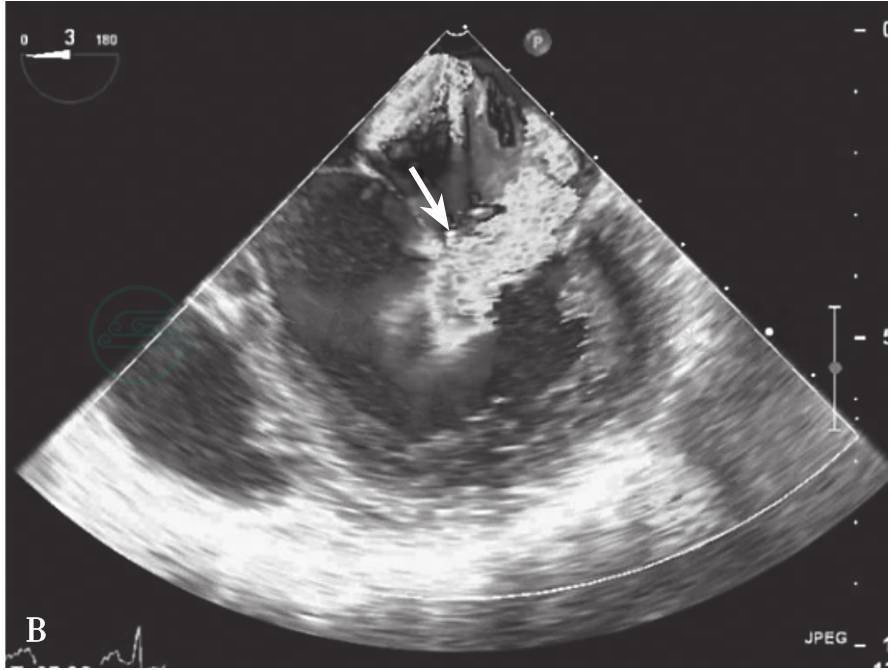
图6-12 5腔心切面显示二尖瓣前叶A1区脱垂

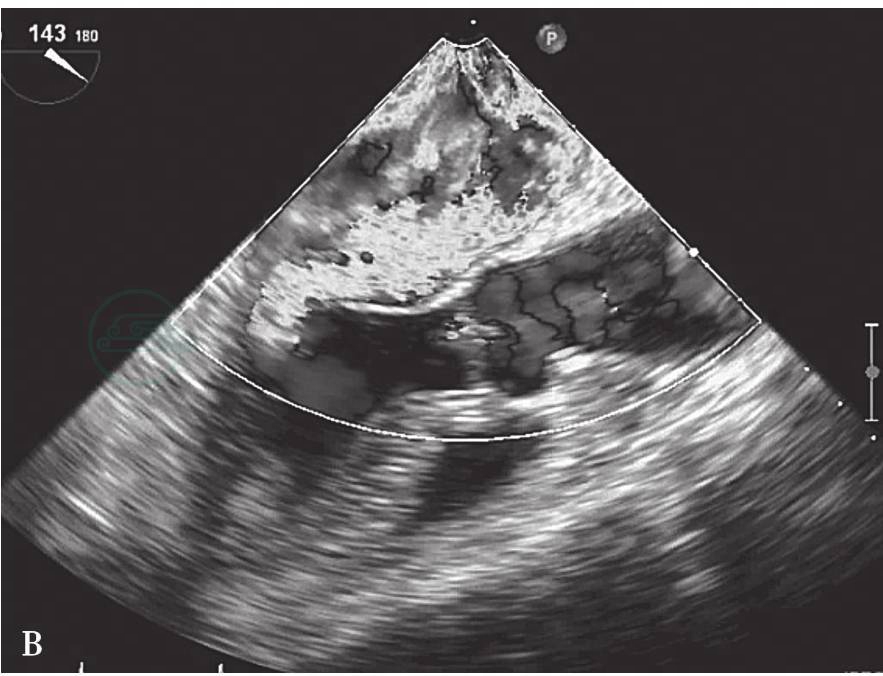
图6-13 食管中段左心室长轴切面显示二尖瓣后叶P2区腱索断裂并脱垂
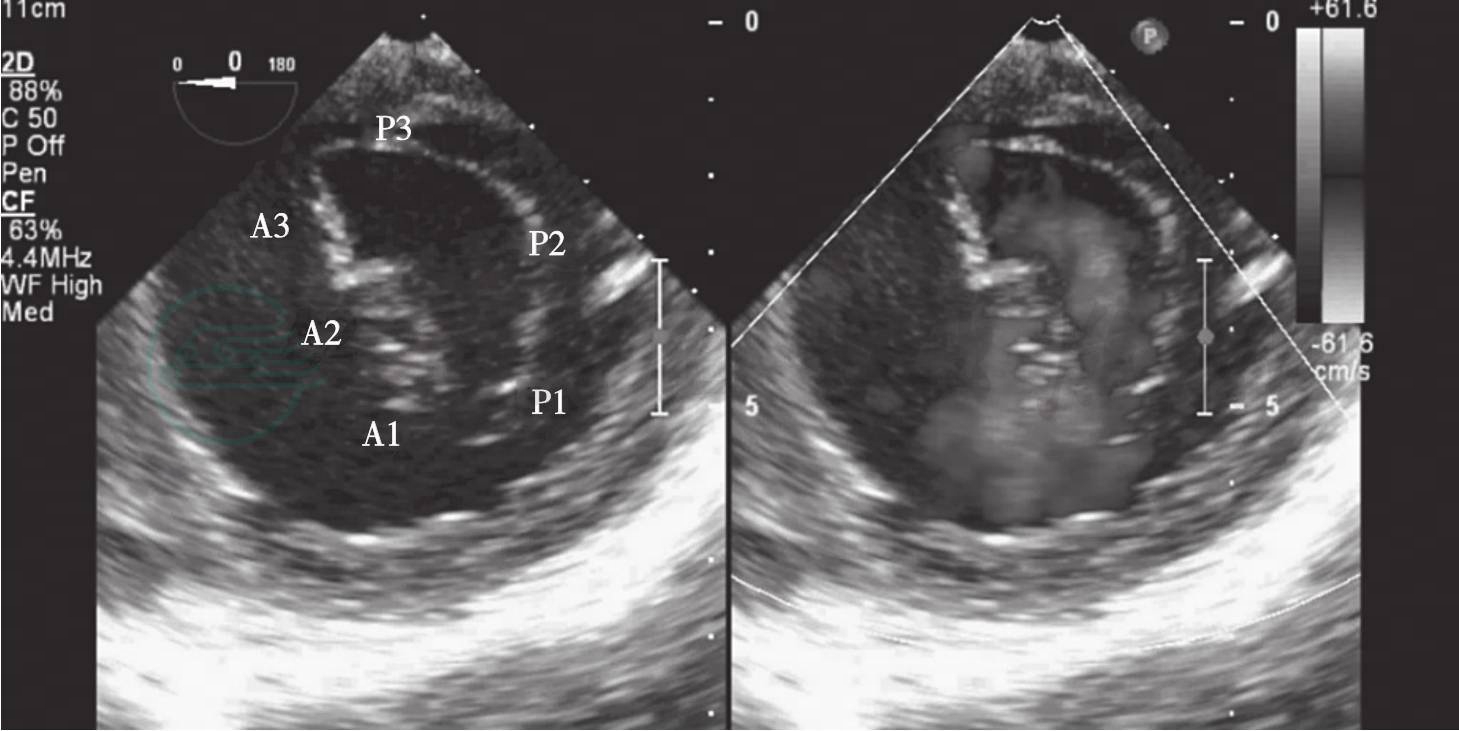
图6-14 经胃底基底段短轴切面。示二尖瓣前后叶,P3区位于“扇形”的顶点
表6-5 不同二维TEE切面所显示的二尖瓣小叶分区
二尖瓣环是一个空间立体环,形状近似“马鞍形”,美国超声心动图学会指南建议应用4腔心切面于舒张中期测量二尖瓣环径,并应用圆形公式来计算瓣环面积,但是这种计算方法简化了瓣环的复杂结构。本文推荐应用左室长轴和交界区切面测量二尖瓣瓣环径,计算二尖瓣环面积。左心室长轴测量二尖瓣环径时,应仔细观察二尖瓣瓣叶的附着点。而这种相互垂直的两个平面在多平面或三维超声(图6-15,图6-16)上很容易得到。
应用经食管实时三维超声心动图评价二尖瓣对以下情况很有帮助:确定病变的部位和范围;确定瓣膜功能异常的机制和程度;与外科医生直接交流超声检查结果,有利于手术计划的制定。另外,实时三维超声有利于判断累及多个小叶的脱垂,对于交界区的病变和瓣叶裂更具有帮助。
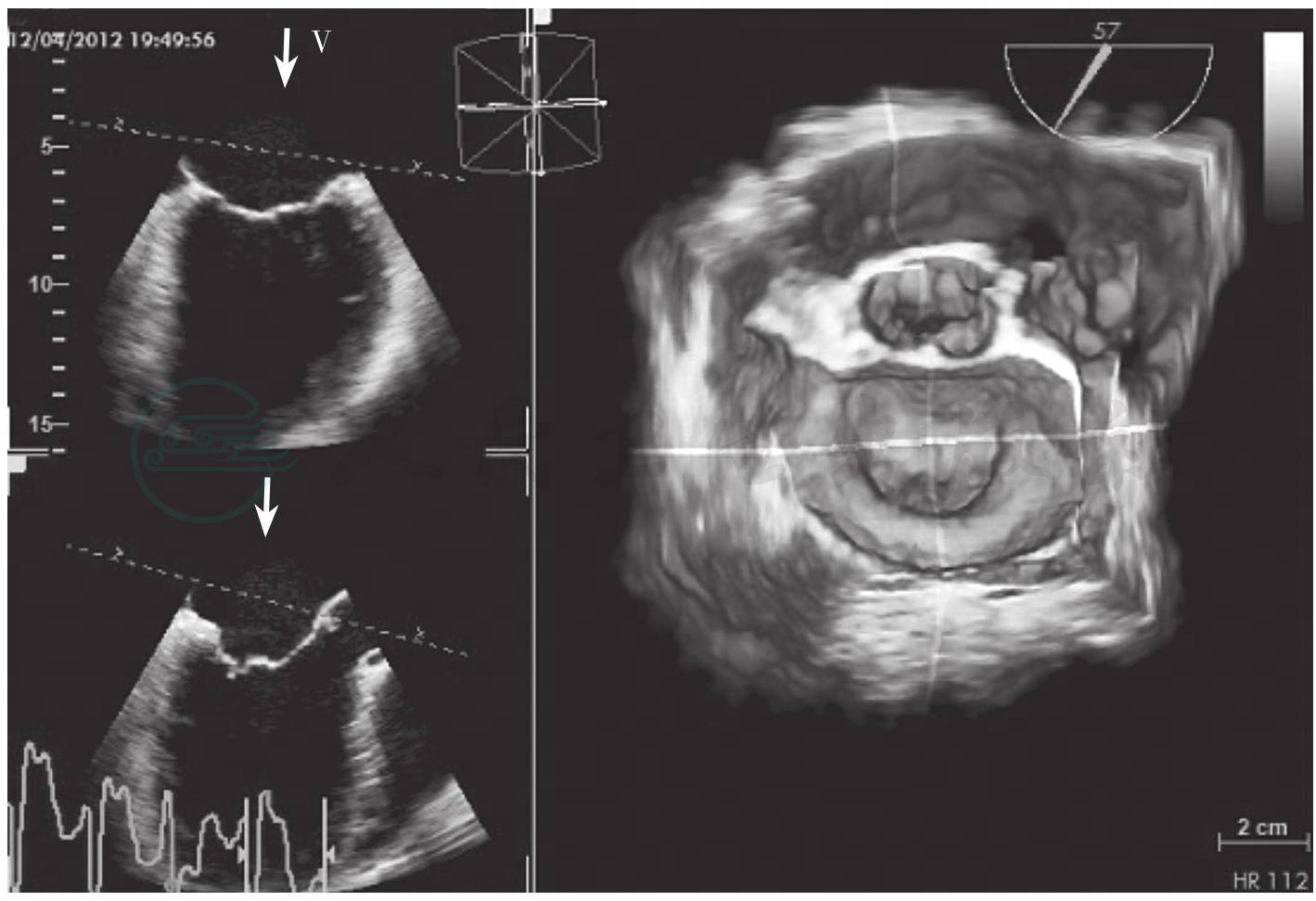
图6-15 正常二尖瓣2个相互垂直平面

图6-16 二尖瓣P2脱垂2个相互垂直平面
十二、TEE-Focus循环病理类型的超声形态特征
参考正常值,就可以对常见的循环系统病理类型进行区分和归纳,从而找到常见的循环系统病理类型的超声形态特征与常见病理类型的关系。
1.休克的超声心动图表现
休克是最常见的循环系统病理类型之一,不同类型的休克超声心动图表现不同,评价指标也不外乎心腔大小,室壁舒缩,瓣膜功能,动静脉血流等。表6-6总结了上述指标在不同休克类型中的表现。
2.心室腔小,室壁厚
常见于高血压病,主动脉瓣狭窄,左心室流出道梗阻,肥厚型心肌病,心肌糖原沉积病;左心室长轴、左心室短轴切面,可见左心室壁增厚,左心室腔缩小(图6-16)食管中段4腔心、右心室流入-流出道切面及胃底心室短轴切面观察右心室壁增厚,右心室腔缩小,见于法洛四联症,肺动脉闭锁,肺动脉高压。
肥厚心室的顺应性降低,前负荷对心房收缩功能的依赖性增加,心肌氧供对后负荷依赖性增加,硬膜外或腰麻可降低外周血管阻力,如盲目进行麻醉可能带来灾难性后果。一般情况下不需要主动增强心肌收缩力,合并流出道梗阻还要减低心肌收缩力,增加外周血管阻力(图6-17箭头所示)和血容量。
表6-6 休克的超声心动图表现

3.左心室腔扩大,左心室壁变薄、搏动幅度减低
心尖四腔、心室短轴切面,心腔扩大,室壁变薄,搏幅减低,这类心脏左心室舒张末压升高(图6-18箭头所示),造成冠脉灌注压降低,心肌缺血。这类患者若诱导期如出现心跳骤停,心肺复苏极为困难。常见于扩张型心肌病,主动脉瓣反流,缺血性心肌病,容量过负荷等。处理上要保持心率/律稳定,合适的前负荷,减轻后负荷,增强心肌收缩力。
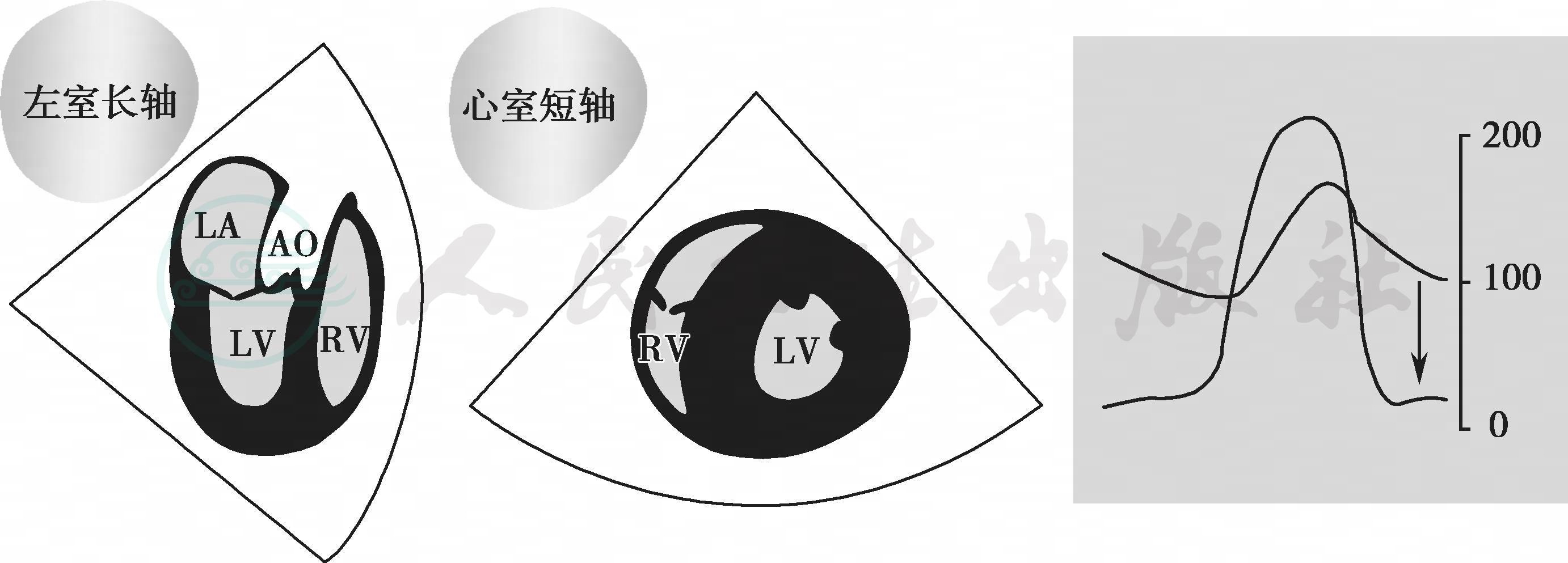
图6-17 室壁增厚,心腔缩小,心室收缩压高于主动脉收缩压
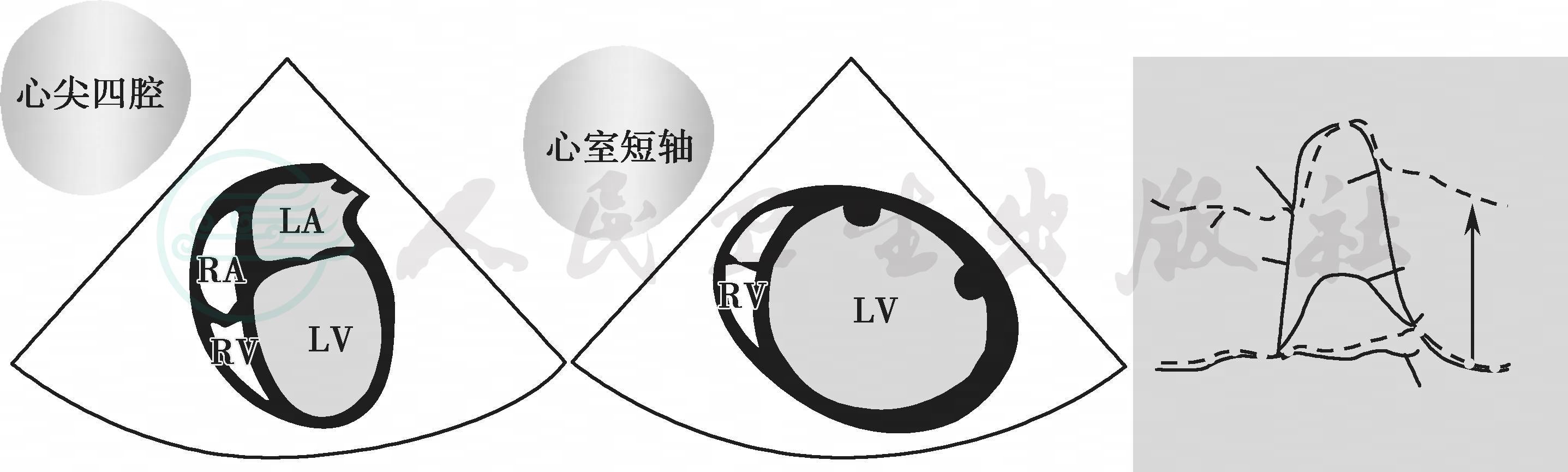
图6-18 左室壁变薄,心腔扩大,左心室舒张末压升高
4.右房右室扩大,左房左室减小
肺栓塞,右室心梗,肺动脉高压,大房缺,二尖瓣狭窄晚期,三尖瓣重度反流,肺静脉异位引流(图6-19)。这类心脏右心室舒张末压升高,如遇到左房压急性升高的因素(急性左心衰、突发心房颤动、二尖瓣急性关闭不全),发生心搏骤停的风险较高。
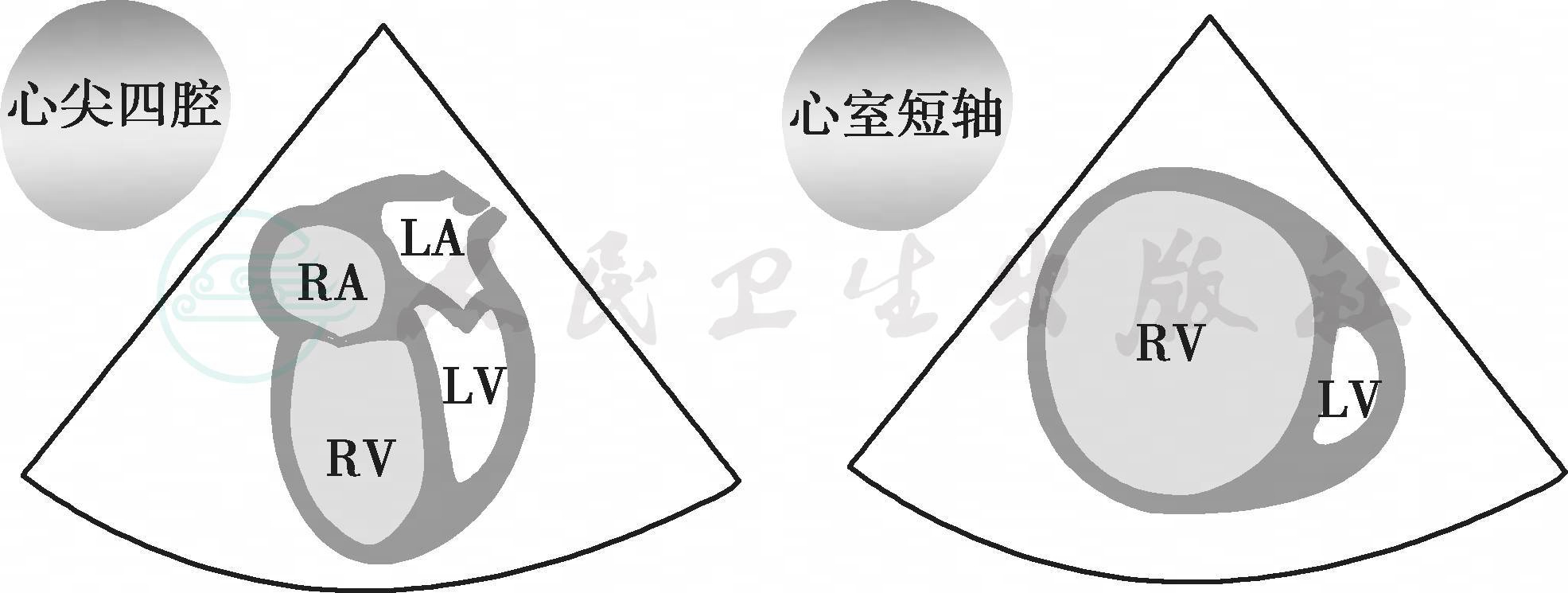
图6-19 右心扩大,左心室容量不足,右心室舒张末压升高
十三、常见心脏病的超声影像特征
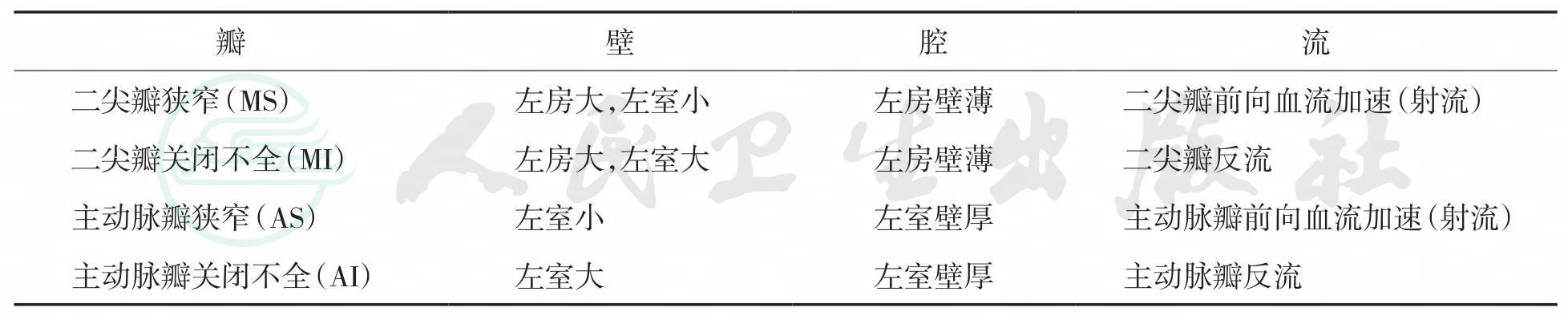
1.单纯瓣膜病的超声影像特征
单纯瓣膜病术中管理风险由大到小依次为:主动脉瓣反流,主动脉瓣狭窄,二尖瓣反流,二尖瓣狭窄。其超声影像特征见表6-7。
表6-7 单纯瓣膜病的超声影像特征
2.二尖瓣反流的Carpentier分型
推荐按照Carpentier建议的根据二尖瓣瓣叶的活动度对MR进行分型(图6-20),Ⅰ型反流为中心性,瓣环扩大,瓣叶运动无受限,腱索无增长或缩短; Ⅱ型反流为偏心性, 瓣叶运动过度,腱索冗长或断裂,瓣环无扩大;Ⅲ型为瓣叶运动限制型,其中Ⅲa型为瓣叶运动自限,腱索由于病变发生融合、短缩,影响瓣膜开闭;Ⅲb型为瓣叶运动受限,腱索本身没有病变,由于左心室扩大或室壁瘤形成,乳头肌随室壁牵拉腱索,导致二尖瓣关闭受限。
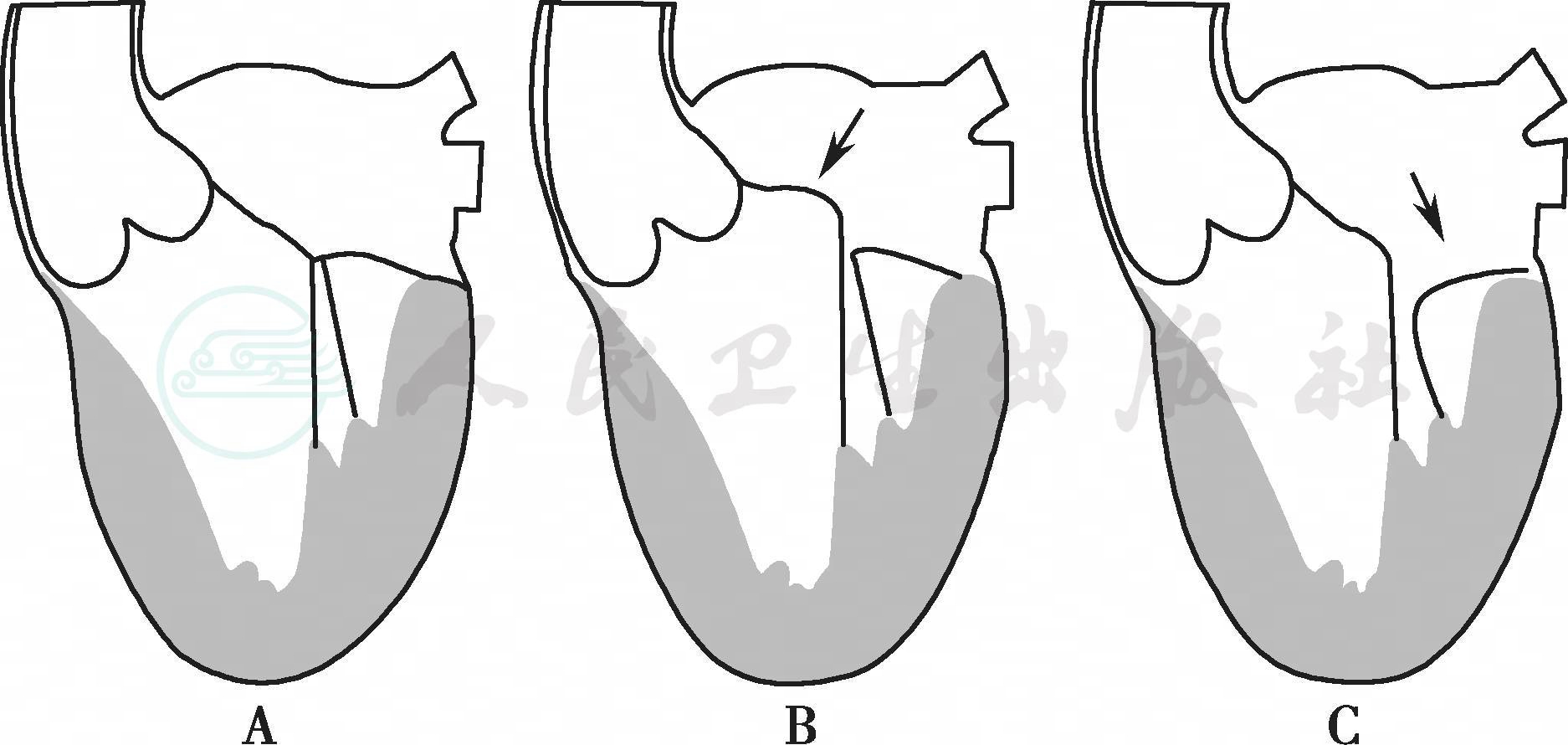
图6-20 I型:瓣叶活动正常,二尖瓣反流呈中心性;Ⅱ型:二尖瓣瓣叶活动过度,二尖瓣反流偏向健侧;Ⅲ型:二尖瓣活动受限,又分为Ⅲa(结构性)和Ⅲb(功能性)两个亚型
3.二尖瓣反流的严重程度评价
MR的严重程度分为微量,轻度,中度,重度,这与血管造影的1+,2+,3+,4+相对应(表6-8)。心脏的二维超声检查常常可以提供明显MR的线索。这些线索可以是直接的,例如较大的对合缺失或瓣叶的结构异常;也可以是间接的,例如重度MR的血流动力学后果为左房左室容量负荷过重,或肺动脉高压的征象(右室扩张,右室肥厚,室间隔平坦,肺动脉扩张,三尖瓣反流)。
反流束最窄的部分,称为“缩流颈(vena contracta)”,可以通过测量缩流颈的直径(图6-21)来判断反流的程度,当直径≥5.5mm时,与心导管测量的重度反流相关性很好。如果使用7mm作为重度MR的截断值会更有帮助,此时特异性强,但敏感性大幅下降。
表6-8 二尖瓣反流的多普勒和定量参数
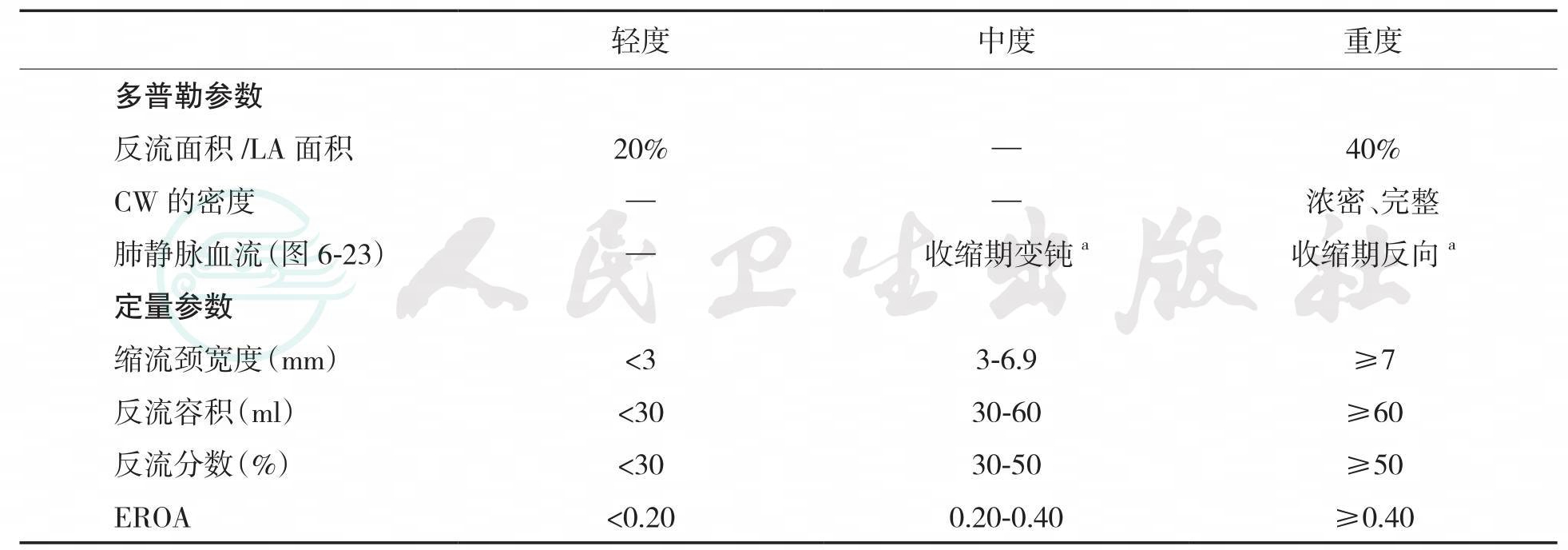
a收缩期变钝和收缩期反向具有特异性但敏感性不高。LA:左房;CW:连续多普勒;EROA:有效反流口面积(图6-22)
反流束的方向也很重要,其不仅仅是病因学的线索,也是严重程度的一个征象。中心性反流可由瓣环扩张或心室功能不全引起,偏心性反流(图6-22)常常由二尖瓣结构本身异常引起的,偏心性的贴壁反流束应该认为是中度以上的。
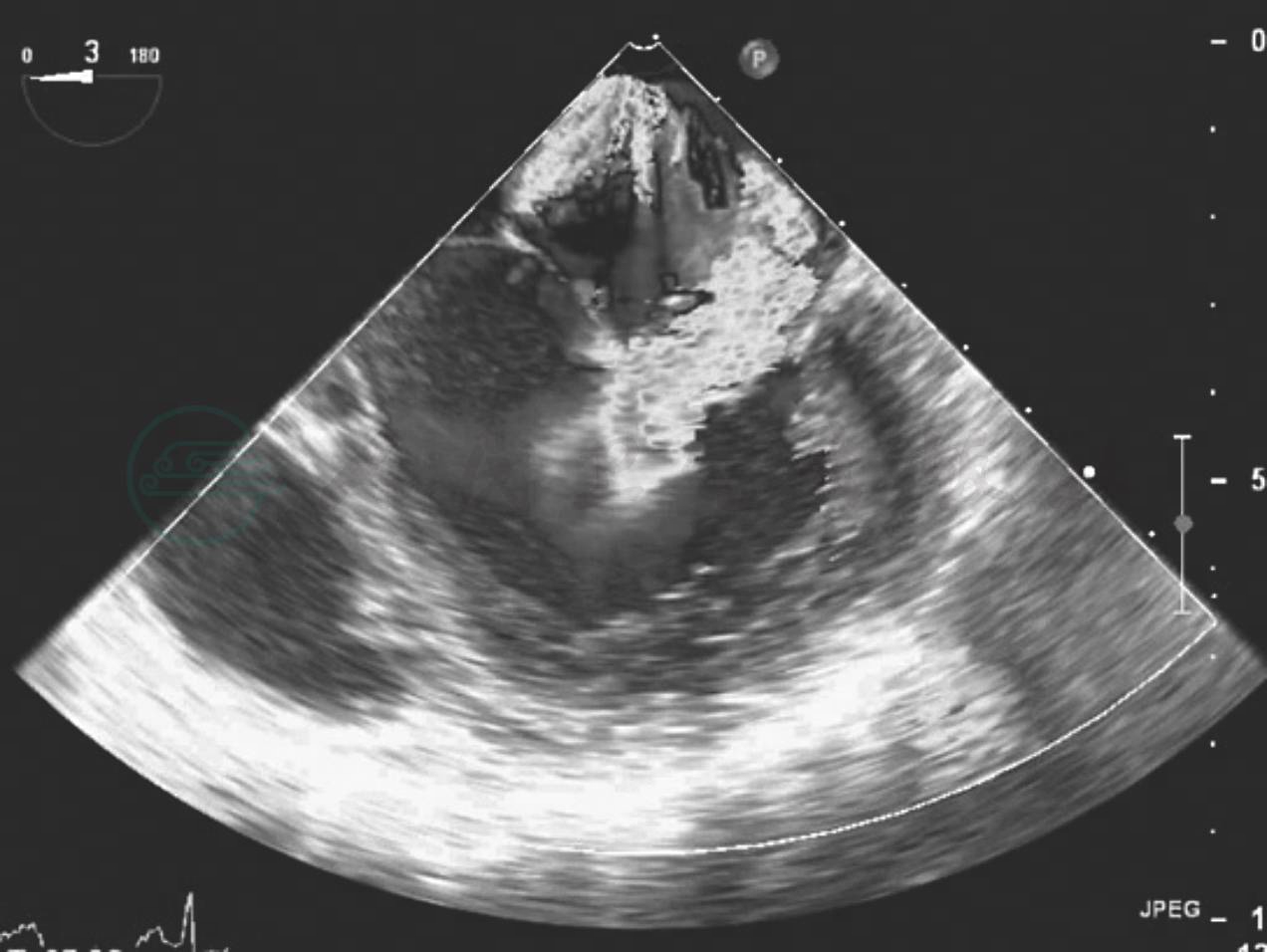
图6-21 缩流颈的测量食管中段4腔心切面,反流束基底部宽度与二尖瓣反流的严重程度相关
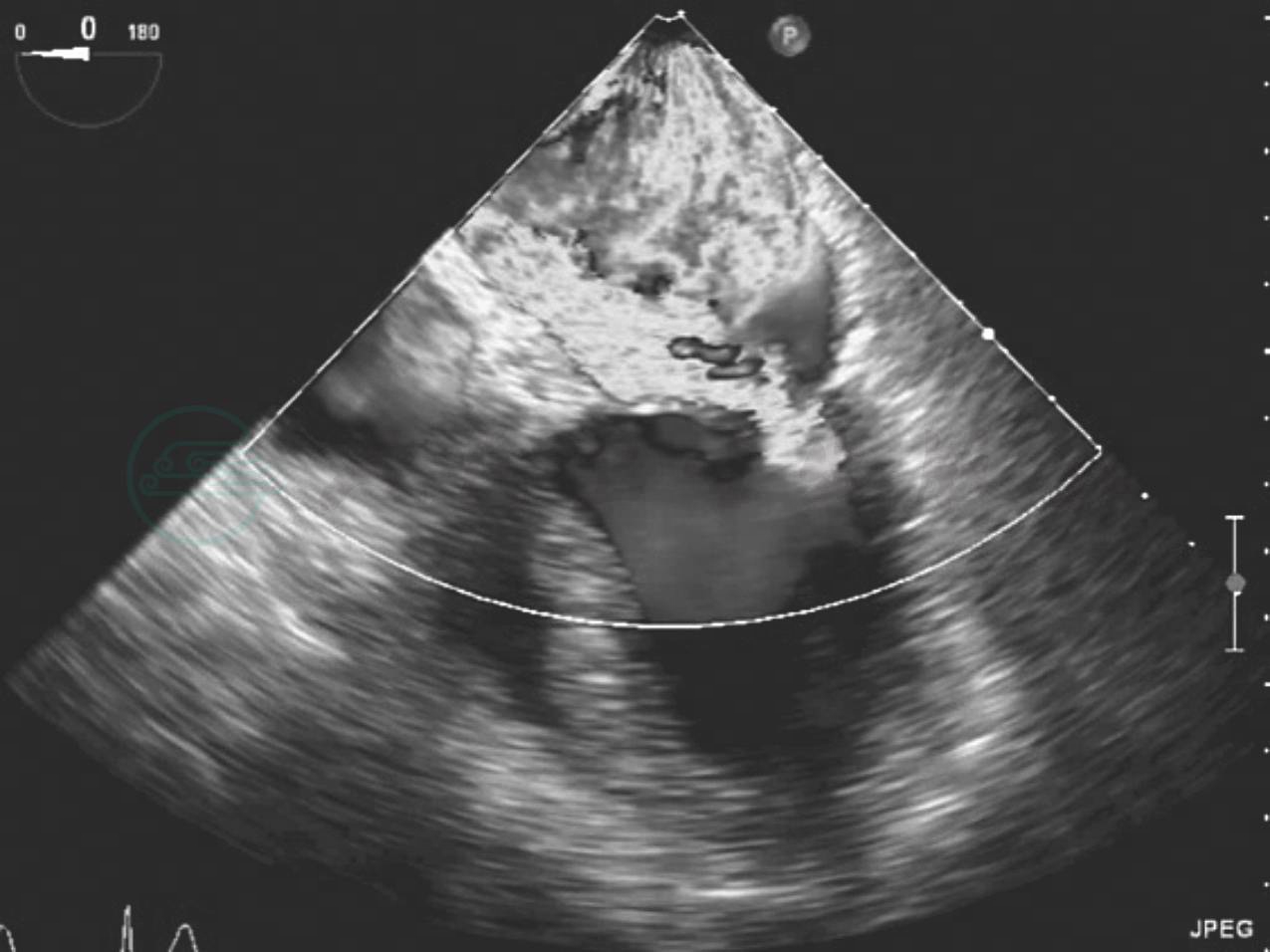
图6-22 偏心性二尖瓣反流
食管中段4腔心切面二尖瓣彩色多普勒血流成像,可见重度MR沿左房内侧壁走行达房顶部
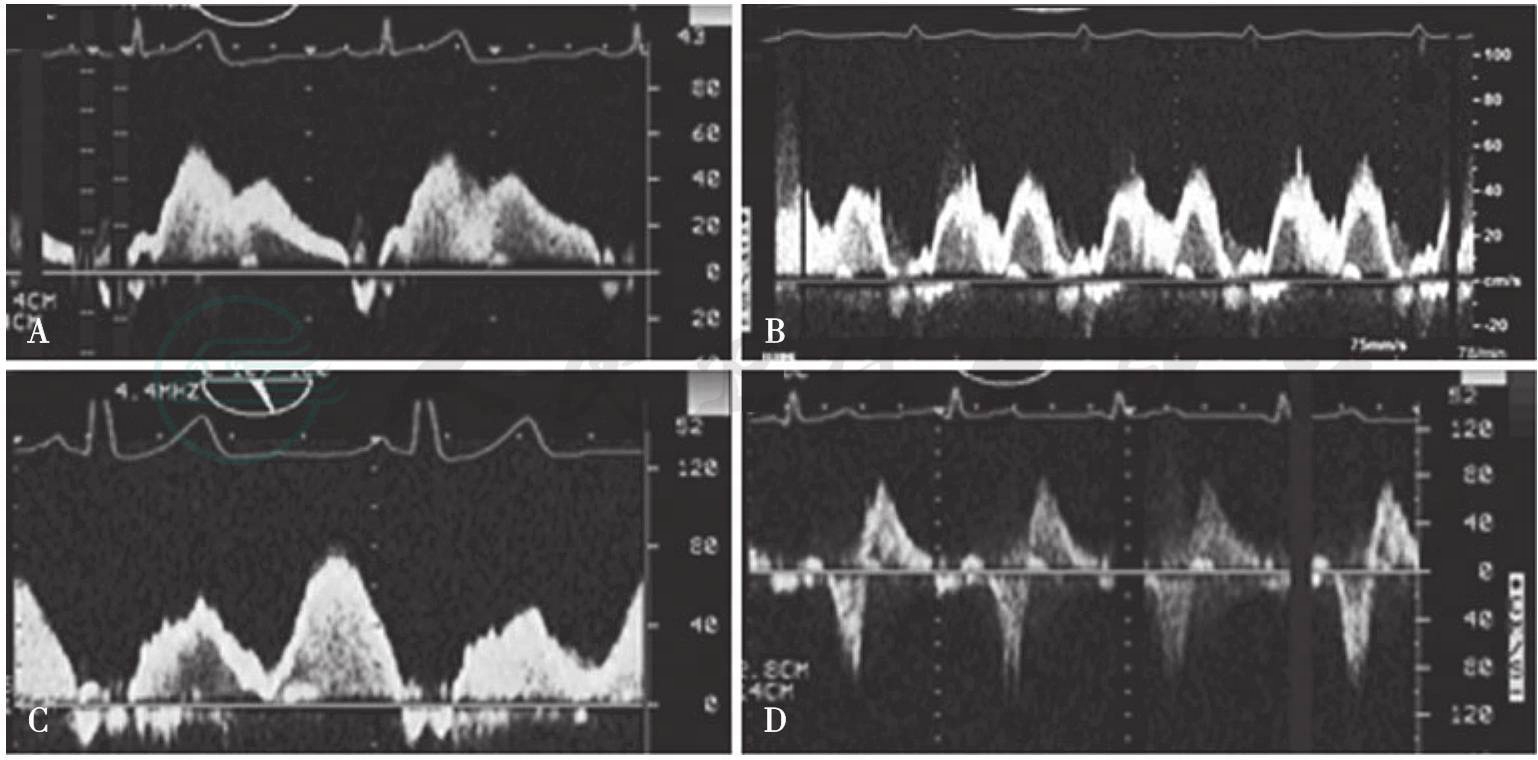
图6-23 二尖瓣反流的肺静脉频谱:A.无反流;B.轻度反流;C.中度反流;D.重度反流引自:Ann Cardiothorac Surg. Nov 2013; 2(6): 796-802.
在上述的评价方法中,没有一种方法自身足以诊断重度MR,但是作为一组评价方法,它们可以提高诊断的准确性。
4.功能性二尖瓣反流
二尖瓣瓣叶结构正常时,也可以存在MR,称为“功能性MR”。功能性MR常出现在长期左室功能不全的患者。病变因素包括以下几个方面:
(1)节段性室壁运动异常和室壁局部扩张(常为室壁瘤)常累及左室的前壁和下壁。左室的几何形状重塑而且左室的球形度增加。
(2)左室和二尖瓣器之间的关系不匹配会导致两组乳头肌之间的距离增加,而且,乳头肌相对于瓣叶的方向发生改变。
(3)上述情况可以导致二尖瓣瓣叶受到牵拉,最终使瓣叶对合受累引起关闭不全。
(4)瓣环扩张,常发生在瓣环的前后径。
(5)心室功能下降,二尖瓣收缩期闭合力降低对瓣叶对合不良也发挥重要的作用。
术前是评价功能性MR最佳时间。如前面提到的,普通麻醉影响心脏负荷状态,在麻醉状态下低估MR程度。结构性MR情况下,麻醉状态下反流看起来似乎不多,但是二尖瓣结构异常仍然存在。然而在功能性MR,几乎不存在二尖瓣结构的异常,那么负荷状态降低可能误导临床医生没有矫正反流程度,这对患者的预后不利。
术中TEE是决定二尖瓣外科手术方案不可缺少的一部分,而且,也是评价MR的监护标准。详细全面的二尖瓣检查使我们能够明确二尖瓣病变的性质和确切的部位。
5.主动脉瓣反流定量
主动脉瓣关闭不全的定量或半定量诊断有许多方法。
(1)反流束长度和面积法:测量彩色反流束面积和长度,因反流束常偏心,与室间隔或二尖瓣前瓣相碰,扩散受限制,反流束与正常或狭窄的二尖瓣血流相混叠,故用反流束大小来定量主动脉瓣反流存在一定局限性,只用于粗略判断轻度和重度反流。
(2)反流束面积/左室流出道截面积,方法为在胸骨旁主动脉瓣短轴切面彩色血流显像显示反流束的面积,同时测出左室流出道面积。
(3)瓣口反流束宽度/左室流出道宽度之比是较实用的方法。于食管中段左心长轴切面,在左室流出道与主动脉瓣环交接处测量反流束宽度和左室流出道最大宽度。此方法能准确地判断90%以上患者的主动脉瓣反流的严重程度,是临床最常采用的方法(表6-9)。
表6-9 主动脉瓣反流定量

JW-反流束宽;LVOTW-左室流出道宽度;JA-反流束面积;LVOTA-左室流出道面积
6.TEE-Focus先心病超声影像特征
常见的先天性疾病按照病理生理学特征可分为两种类型,“肺充血”型和“肺缺血”型(表6-10)。两类疾病TEE检查要点和诊疗要点见下述:
表6-10 按肺动脉血流将先天性心脏病分为两大类

(1)以肺充血为主要表现的先天性心脏病的超声影像特征:房间隔缺损,室间隔缺损,动脉导管未闭,主、肺动脉窗等疾病。早期表现为左向右分流(图6-24中带箭头实线所示),胸片显示肺纹理增多,虚线表示相应心血管节段存在“无效循环”,“无效循环”经过的心血管腔一般要扩大,“无效循环”未经过的心血管腔一般不扩大,超声影像基本特征见表6-11。
肺充血后血管床扩张,容易发生感染和急性肺动脉高压危象,体外循环术后容易发生鱼精蛋白过敏,严重者甚至会发生心脏停搏。房间隔缺损、室间隔缺损、动脉导管未闭的患者长期肺充血可导致肺动脉高压,肺小动脉管壁增厚、闭塞直至艾森曼格综合征。艾森曼格综合征的患者行剖宫产手术时要注意维持体循环阻力和血容量,降低肺循环阻力。
(2)以肺缺血为主要表现的典型先天性心脏病有:法洛四联症、肺动脉闭锁等(表6-10)。这类疾病肺血管树发育差,胸片肺纹稀疏,早期表现为右向左分流,术中血氧饱和度下降的原因是体循环阻力下降,右向左分流增加,肺血减少,表现为“血压依赖性氧合”,如遇到右室流出道动力性梗阻,会出现严重的低氧血症,称为缺氧发作。“肺血少”的先心病通常无肺动脉高压,不容易发生鱼精蛋白过敏,不发生艾森曼格综合征,左房压低,左心室容积偏低,术后需要避免容量过负荷。这类患者因为肺缺血,因此吸入麻醉效果差,由于在发育期间形成了大量的体肺侧支(MAPCUS),增加肺血流量,这些侧支循环在术后常会带来间质性肺水肿,因此需要做杂交手术,在矫正肺动脉狭窄/闭锁的同时行侧支封堵。
十四、小结
TEE监测要根据临床和教学的实际需要制定标准和规范,并持续改进,学科之间的协作已经成为TEE超声检查临床、教学、科研、管理工作的新特点,不仅有超声学会和麻醉学会两个学科之间的协作,也有包括心脏学会在内的三个学科之间的协作,TEE临床推广与各学会的专科准入制度的结合。
围手术期TEE检查要在临床中实现规范化、标准化,基本的思路是:发现TEE影像的特征,建立个体化的病理生理学模型,结合相关诊疗经验和循证医学证据进行术中诊疗决策,管理和控制围手术期风险。
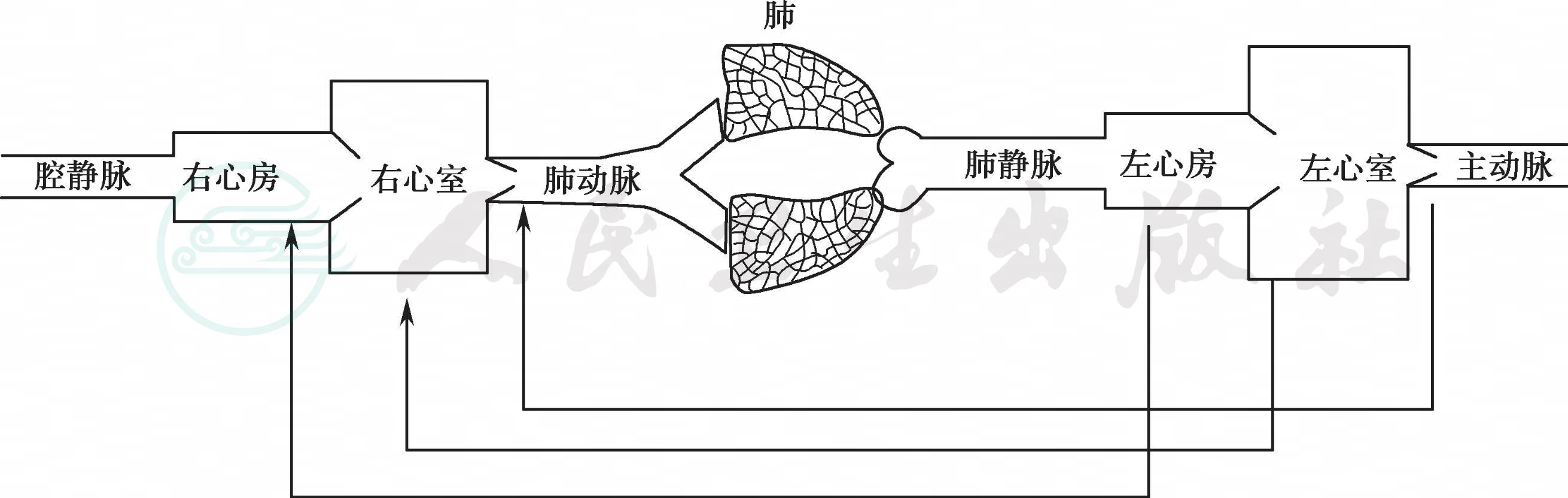
图6-24 TEE-Focus分流性先心病病理生理模式图
表6-11 常见肺充血型先天性心脏病的超声影像特征

对于非心脏专科麻醉医师,超声快速监测和评价心血管功能将使危重患者和重、大手术的围手术期管理变得更加安全,对心血管专科麻醉医师和ICU医师,TEE在围手术期能提供有关心脏及大血管结构与功能的实时动态信息,有助于帮助手术团队进一步明确术前诊断,发现新的形态及功能异常,调整麻醉和外科、急危重症的决策,评估、监控手术风险、随访手术效果。
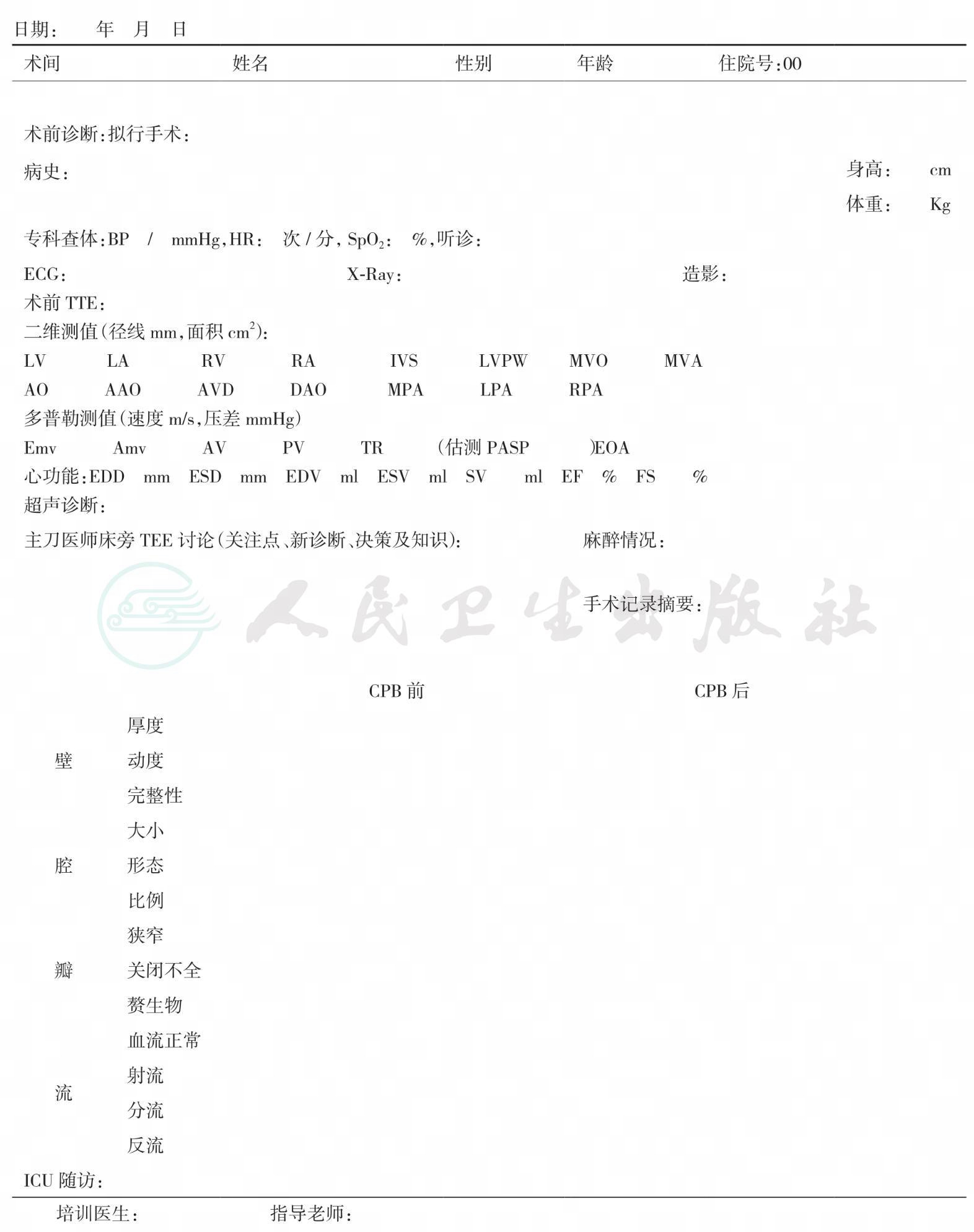
附件:术中TEE监测记录单
1. Cahalan MK,et al. Practice guidelines for perioperative transesophageal echocardiography. A report by the American Society of Anesthesiologists and the Society of Cardiovascular Anesthesiologists Task Force on Transesophageal Echocardiography. Anesthesiology,1996,84(4):986-1006 .
2. Shanewise JS,Cheung AT,Aronson S. et al. ASE/SCA guidelines for performing a comprehensive intraoperative multiplane transesophageal echocardiography examination:recommendations of the American Society of Echocardiography Council for Intraoperative Echocardiography and the Society of Cardiovascular Anesthesiologists Task Force for Certification in Perioperative Transesophageal Echocardiography. Anesth Analg,1999,89(4):870-884 .
3. Shiga T,Ogawa R. Five-grade scoring system is still confusing:does ASE/SCA set up a double standard? Anesth Analg,2000,90(5):1248-1249.
4. Cahalan MK,Abel M,Goldman M,Pearlman A,Sears-Rogan P,Russell I,Shanewise J,Stewart W,Troianos C,American Society of Echocardiography,Society of Cardiovascular Anesthesiologists. American Society of Echocardiography and Society of Cardiovascular Anesthesiologists task force guidelines for training in perioperative echocardiography. Anesth Analg,2002,94(6):1384-1388 .
5. Cheitlin MD,Armstrong WF,Aurigemma GP,et al. ACC/AHA/ASE 2003 guideline update for the clinical application of echocardiography:summary article:a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (ACC/AHA/ ASE Committee to Update the 1997 Guidelines for the Clinical Application of Echocardiography). Circulation,2003,108:1146-1162.
6. Mathew JP,Glas K,Troianos CA,Sears-Rogan P,Savage R,Shanewise J,Kisslo J,Aronson S,Shernan S,American Society of Echocardiography,Society of Cardiovascular Anesthesiologists. American Society of Echocardiography/ Society of Cardiovascular Anesthesiologists recommendations and guidelines for continuous quality improvement in perioperative echocardiography.J Am Soc Echocardiogr,2006,19(11):1303-1313.
7. American Society of Anesthesiologists and Society of Cardiovascular Anesthesiologists Task Force on Transesophageal Echocardiography. Practice guidelines for perioperative transesophageal echocardiography:An updated report by the American Society of Anesthesiologists and the Society of Cardiovascular Anesthesiologists Task Force on Transesophageal Echocardiography. Anesthesiology,2010,112:1084-1096.
8. Song H,Peng YG,Liu J. Innovative transesophageal echocardiography training and competency assessment for Chinese anesthesiologists:role of transesophageal echocardiography simulation training. Curr Opin Anaesthesiol,2012,25(6):686-669.
9. Reeves ST,Finley AC,Skubas NJ,Swaminathan M,Whitley WS,Glas KE,Hahn RT,Shanewise JS,Adams MS,Shernan SK,Council on Perioperative Echocardiography of the American Society of Echocardiography,Society of Cardiovascular Anesthesiologists. Basic perioperative transesophageal echocardiography examination:a consensus statement of the American Society of Echocardiography and the Society of Cardiovascular Anesthesiologists. J Am Soc Echocardiogr,2013,26(5):443-456.
10. Hahn RT,Abraham T,Adams MS,et al. Guidelines for performing a comprehensive trans-esophageal echocardiographic examination:recommendations from the American Society of Echocardiography and the Society of Cardiovascular Anesthesiologists. Anesth Analg,2014,118(1):21-68.
11. Vincent JL,De Backer D. Circulatory shock. N Engl J Med,2013,31(18):1726-1734.
12. Leung JM,Levine EH. Left ventricular end-systolic cavity obliteration as an estimate of intraoperative hypovolemia. Anesthesiology,1994,81(5):1102-1109.
13. Smith ZA,Wood D. Emergency focussed assessment with sonography in trauma(FAST) and haemodynamic stability. Emerg Med J,2011,31(4):273-277.
14. Jensen MB,Sloth E,Larsen KM,Schmidt MB. Transthoracic echocardiography for cardiopulmonary monitoring in intensive care. Eur J Anesthesiol,2004,21(9):700-707.
15. Pai RG,Bansal RC,Shah PM. Doppler-derived rate of left ventricular pressure rise. Its correlation with the postoperative left ventricular function in mitral regurgitation. Circulation,1990,82(2):514-520.