11.4: El cerebro y el sueño
- Page ID
- 148320
- Describir el papel de los pones, la médula, el hipotálamo (SCN), el tálamo, el prosencéfalo basal y la glándula pineal en la iniciación y mantenimiento del sueño.
- Analizar el papel de diferentes neuroquímicos, particularmente el neurotransmisor inhibidor GABA y la hormona del sueño melatonina en el inicio y mantenimiento del sueño.
- Contraste el papel de otros neuroquímicos como los neurotransmisores excitadores glutamato y norepinefrina en la vigilia y el sueño.
Visión general
En general, hay varias regiones del cerebro que trabajan en concierto para aumentar la vigilia y la excitación, o para hacer que nos quedemos dormidos o permanezcamos dormidos. Los neurotransmisores excitadores primarios como el glutamato y la acetilcolina y el neurotransmisor inhibidor primario GABA juegan un papel en estos procesos.
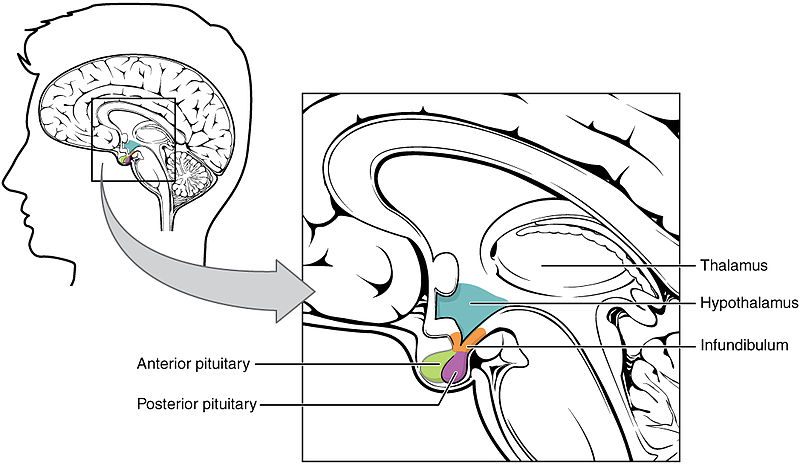
Durante la gripe española de 1918 algunos pacientes entraron en coma y algunos quedaron sin dormir antes de morir. Von Economo realizó autopsias y encontró diferentes tipos de lesiones. Concluyó que el hipotálamo posterior/parte superior del mesencéfalo podría ser un centro de vigilia, y el área preóptica del hipotálamo anterior podría ser un centro del sueño. Estas áreas se ilustran en la Figura\(\PageIndex{1}\). Posteriormente innumerables autopsias sugieren que cuando uno entra en coma, su tronco encefálico ha sufrido daños.
El sueño no es un estado de silencio neuronal
El trabajo de Moruzzi y Magoun (1949) también sugirió que cuando se destruyó la formación reticular de los gatos, se desencadenaron los comas, y estimular esta parte llevó al despertar del sueño normal. Además, dado que esta parte recibe mensajes entrantes a través de vías sensoriales, desarrollaron el concepto de “sistema reticular activante ascendente” o el principal contendiente para el “centro de vigilia”.
Pero estos experimentos iniciales tuvieron varios problemas. Dado que las sustancias neurotóxicas que se utilizaron para destruir las neuronas/cuerpos celulares del hipotálamo posterior y la formación reticular mantuvieron intactos los axones que se originaron en otros lugares, la función de vigilia que se disminuyó inicialmente, rápidamente volvió a la normalidad.
Lo más importante es que estos estudios también mostraron que el sueño no es un proceso pasivo, en el que ser privado de la entrada sensorial provoca sueño. Mucha gente cree que dormir es algo que sucede en ausencia de cualquier otra cosa como cuando alguien está aburrido. Por ejemplo, los estudiantes de medicina que asistan a una conferencia sobre una materia que no les interesa totalmente se caerán a dormir. No obstante, es importante tener en cuenta que eso no es en realidad lo que está sucediendo. Si un grupo de niños de siete años que habían dormido lo suficiente las noches anteriores estuvieran sentados en la misma conferencia, ¡no se quedarían dormidos sino que estarían rebotando en las paredes!
En estudios posteriores, la aplicación de estímulos eléctricos al tálamo de los gatos cuando estaban despiertos provocó que se durmieran. Esto indica que el sueño implica interacciones entre el tálamo y la corteza. Además, cuando se descubrió que los ciclos de sueño y vigilia no se vieron alterados por la activación sensorial y que durante el REM hay una actividad intensa en la corteza, la idea del sueño como pasividad se desacreditó aún más.
Hay dos circuitos neuronales principales en el tronco encefálico que operan en oposición y alternancia entre sí. Uno de estos circuitos estimula la vigilia, el otro estimula el sueño, y su interacción está regulada por el reloj interno del cuerpo (SCN).
Algunas grandes áreas de la corteza están así bajo el control de estas redes de pequeños grupos de neuronas que se localizan en el tronco encefálico y que forman circuitos complejos, no solo “centros de sueño” o “centros de vigilia”. La vigilia, indispensable para la supervivencia, está así asegurada por toda una red de estructuras redundantes.
Regiones del prosencéfalo involucradas en el sueño
En la Figura se\(\PageIndex{1}\) puede ver el hipotálamo donde se ubica el área específica del cerebro, el núcleo supraquiasmático (SCN- que está involucrado en la regulación del ritmo diario/circadiano del cuerpo).
Hipotalálamo anterior/SCN
SCN
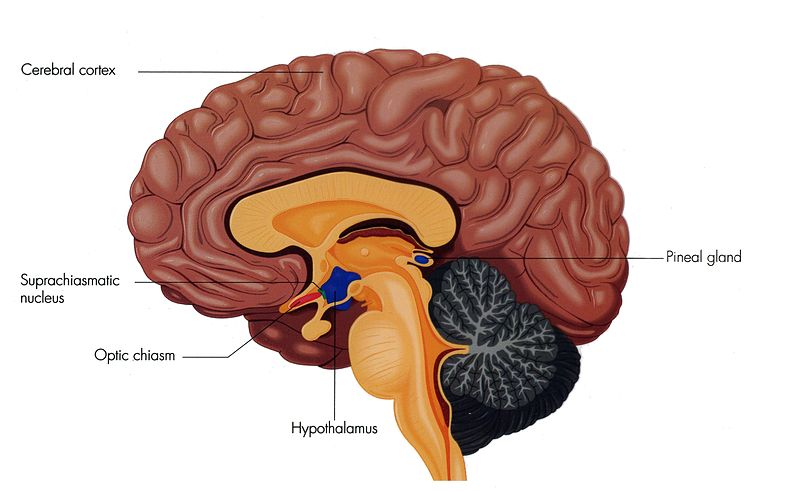
El SCN se considera “reloj interno del cuerpo”. Se discutirá en una sección posterior con más detalle. El SCN es una estructura bilateral localizada en la parte anterior del hipotálamo. Es el marcapasos central del sistema de cronometraje circadiano y regula la mayoría de los ritmos circadianos en el cuerpo (Hastings et al, 2018). El SCN recibe señales de muchos lugares diferentes. El principal es el tracto retinohipotalámico que se origina a partir de células ganglionares fotosensibles (sensibles a la luz) de la retina. El SCN envía señales a estructuras como la glándula pineal, produciendo melatonina durante la noche para la inducción del sueño. Se ha encontrado que las alteraciones en el sistema circadiano SCN se correlacionan con diversos trastornos del estado de ánimo y trastornos del sueño.
Área preóptica
El hipotálamo anterior también juega un papel fundamental en el proceso de conciliar el sueño. Esta estructura, y en particular su área preóptica, parece ser sensible a la serotonina liberada durante los períodos de vigilia. Al parecer, cuando la serotonina estimula esta zona preóptica del hipotálamo anterior, sus neuronas GABAérgicas (productoras de GABA) a su vez inhiben el hipotálamo posterior, fomentando así el sueño. Se sabe que el daño a estas neuronas GABAérgicas causa insomnio, mientras que estimularlas hace que los sujetos experimentales se duerman rápidamente.
Interruptor de sueño-vigilia
Los experimentos in vitro han indicado que los neurotransmisores promotores de la vigilia serotonina, norepinefrina y acetilcolina inhiben las neuronas GABA preópticas identificadas (Gallopin et al., 2000); por lo tanto, interacciones mutuamente inhibidoras entre la región preóptica promotora del sueño y el hipotalámico relacionado con la excitación y las estructuras del mesencéfalo pueden proporcionar un sustrato para un “interruptor de sueño-vigilia” (McGinty y Szymusiak, 2000; Saper et al., 2001). Así, la activación de las células preópticas promotoras del sueño podría conducir al inicio del sueño al inhibir las estructuras de excitación; a su vez, la activación de las estructuras hipotalámicas y mesencéfalo de excitación podría suprimir la actividad de las células preópticas promotoras del sueño NREM, así como de las neuronas promotoras de REM-( Reinoso-Suárez et al., 2010) y facilitar el cambio a la vigilia.
Hipotálamo posterior
La estimulación del hipotálamo posterior produce un estado de vigilia comparable al inducido por la estimulación de la formación reticular en el tronco encefálico. La actividad del hipotálamo posterior disminuye de forma natural durante el sueño, cuando libera menos histamina, molécula que utiliza como neurotransmisor. Se sabe que los antihistamínicos que toman las personas para los síntomas de alergia causan cierta somnolencia, al reducir la actividad de la histamina.
Tálamo
El tálamo contiene neuronas que envían proyecciones a lo largo de la corteza. La activación de estas neuronas talamocorticales hace que liberen aminoácidos excitadores como el aspartato y el glutamato, contribuyendo así a la excitación de la corteza y a la vigilia. Durante la vigilia, estas neuronas generan potenciales de acción única a intervalos regulares. Sin embargo, a medida que el individuo se duerme, estas neuronas comienzan a disparar en ráfagas, haciendo así que la corteza muestre el patrón de EEG sincronizado que es típico del sueño (ver sección * para las etapas del sueño).
Prosencéfalo basal
El sistema del prosencéfalo basal está compuesto por neuronas que sintetizan acetilcolina y/o GABA. Por sí mismas, estas neuronas representan el 70% de la inervación colinérgica de la corteza (donde la corteza es activada por la acetilcolina), al tiempo que envían proyecciones a los núcleos talámicos. Estimular estas neuronas provoca vigilia, pero destruirlas con sustancias neurotóxicas hace que la vigilia disminuya por muy poco tiempo.
En las situaciones que se acaban de describir, la activación cortical que provoca la vigilia resulta de la estimulación directa de las neuronas corticales por los diversos componentes de la red de vigilia. Pero estas neuronas corticales también se pueden activar de otra manera: por la inhibición de aquellas neuronas que inhiben naturalmente la actividad cortical. Y eso es exactamente lo que hacen las neuronas GABAérgicas localizadas en el hipotálamo posterior y en el prosencéfalo basal: inhiben a otras neuronas gabaérgicas corticales.
Esta red ejecutiva para la vigilia es activada por otros sistemas que surgen en el tronco encefálico.
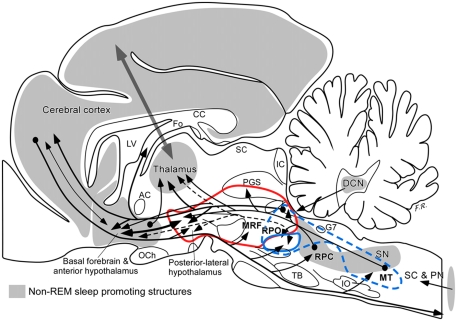
Por lo tanto, todas estas señales de vigilia dejan de llegar a la corteza al inicio del sueño no REM. Se interrumpen en el tálamo, que sirve como un verdadero guardián de la corteza y está muy influenciado por los sistemas neuromoduladores difusos del tronco encefálico. La complejidad de estas interacciones en el sueño NREM se ilustra en el diagrama del cerebro de gato a continuación (Ver Figura\(\PageIndex{2}\)). Este diagrama ilustra un conjunto complejo de conexiones entre estructuras corticales, subcorticales y del tronco encefálico que median diversos aspectos del sueño REM y NREM. La cifra es complicada, y los detalles no son importantes para nuestro propósito aquí. Se incluye para ilustrar la complejidad de las conexiones entre diferentes subestructuras cerebrales y señales que se envían para mantener el movimiento del individuo a través de las diferentes etapas del sueño a lo largo de la noche.
[Una leyenda indica que el complejo o unidad tálamo-corteza cerebral es más oscuro para enfatizar que estas estructuras son necesarias para los signos conductuales y bioeléctricos que caracterizan el sueño NREM. AC: comisura anterior; CC: cuerpo calloso; DCN: núcleos cerebelosos profundos; Fo, fórnix; G7, genu del nervio facial; IC: colículo inferior; IO, olivo inferior; VI, ventrículo lateral; MRF; formación reticular mesencéfalo; MT, tegmento medular; OCh, quiasma óptico; PGS, sustancia gris periacueductal; PC, caudal Núcleo reticular pontino; RPO: núcleo reticular pontino oral; SC, colículo superior; SC y PN, médula espinal y nervios periféricos; SN, núcleo solitario; TB, cuerpo trapezoidal.]
El patrón de actividad rítmica establecido por las neuronas talamocorticales que desconecta la corteza de las señales internas y externas al inicio del sueño no REM. Por el contrario, durante las fases REM del sueño, el tálamo probablemente continúe pasando al menos algunas de estas señales a la corteza, al menos en alguna forma fragmentaria, filtrada o distorsionada.
La regulación de la vigilia es esencial para la supervivencia e involucra varias estructuras redundantes diferentes en el cerebro. Ninguna de estas estructuras, tomadas de forma aislada, es indispensable para la activación de la corteza. Pero tres de estas estructuras cerebrales que envían proyecciones a la corteza son suficientes para mantener el patrón EEG desincronizado que es característico de la vigilia. Estas estructuras son el 1. hipotálamo posterior, 2. los (núcleos intralaminares del) tálamo y 3. el prosencéfalo basal. Juntos a menudo se les conoce como la “red ejecutiva”.
Glándula pineal
Inferior y algo posterior al tálamo es la glándula pineal, una pequeña glándula endocrina cuyas funciones no son del todo claras. Se sabe que las células pinealocíticas que componen la glándula pineal producen y secretan la hormona amina melatonina, la cual se deriva de la serotonina.
La secreción de melatonina varía según el nivel de luz recibida del ambiente. Cuando los fotones de luz estimulan las retinas de los ojos, se envía un impulso nervioso al SCN. Desde el SCN, la señal nerviosa se lleva a la médula espinal y eventualmente a la glándula pineal, donde se inhibe la producción de melatonina. Como resultado, los niveles sanguíneos de melatonina bajan, promoviendo la vigilia. En contraste, a medida que disminuyen los niveles de luz, como durante la noche, la producción de melatonina aumenta, aumentando los niveles sanguíneos y causando somnolencia. La glándula pineal y la melatonina se discuten con más detalle en la sección *
Mire este video para ver una animación que describe la función de la hormona melatonina. ¿Qué debes evitar hacer en medio de tu ciclo de sueño que disminuya la melatonina?
[reveal-answer q=” 598458″] Mostrar respuesta [/revelar-respuesta]
[respuesta oculta a=” 598458″] Encendiendo las luces. [/respuesta ocultada]
La secreción de melatonina puede influir en los ritmos circadianos del cuerpo (discutidos en la sección *), las fluctuaciones de luz oscura que afectan no solo la somnolencia y la vigilia, sino también el apetito y la temperatura corporal. Curiosamente, los niños tienen niveles de melatonina más altos que los adultos, lo que puede impedir la liberación de gonadotropinas de la hipófisis anterior, inhibiendo así el inicio de la pubertad. Finalmente, un papel antioxidante de la melatonina es el tema de investigación actual.
El desfase horario ocurre cuando una persona viaja a través de varias zonas horarias y se siente somnolienta durante el día o despierta por la noche. Viajar a través de múltiples zonas horarias perturba significativamente el ciclo de luz-oscuridad regulado por la melatonina. La síntesis de melatonina puede tardar hasta varios días en ajustarse a los patrones de luz-oscuridad en el nuevo entorno, lo que resulta en jet lag. Algunos viajeros aéreos toman suplementos de melatonina para inducir el sueño.
Regiones del cerebro posterior involucradas en el sueño
Existen varias “regiones inferiores” del tronco encefálico que parecen estar involucradas en la regulación del sueño según investigaciones tempranas y actuales.
Pons
La región del tronco encefálico conocida como pons es crítica para iniciar el sueño REM. Durante el sueño REM, los pones envían señales a los núcleos visuales del tálamo y a la corteza cerebral (esta región es responsable de la mayoría de nuestros procesos de pensamiento). El pons también envía señales a la médula espinal, provocando la parálisis temporal que es característica del sueño REM. Esto es lo que sucede en la experiencia de parálisis temporal del sueño que muchas personas podrían haber experimentado. Como los pons efectivamente todavía están “dormidos” mientras la corteza está “despierta”, ¡las personas experimentan la aterradora incapacidad de mover su cuerpo mientras están completamente conscientes!
Además, las estructuras como el hipotálamo anterior juegan un papel importante en el inicio del sueño.
Médula y RAS
El sistema de activación reticular (RAS) juega un papel importante en la conciencia consciente. Según Iwanczuk y Guzniczak (2015), “El sistema activante reticular ascendente (ARAS) es responsable de un estado de vigilia sostenido. Recibe información de receptores sensoriales de diversas modalidades,... [y esas vías] llegan al tálamo directa o indirectamente... El sistema de activación reticular comienza en la parte dorsal del mesencéfalo posterior y los pones anteriores, continúa hacia el diencéfalo, y luego se divide en dos partes que alcanzan el tálamo y el hipotálamo, que luego se proyectan hacia la corteza cerebral”.
Se cree que la región del núcleo del tracto solitario en la médula dorsal proporciona un vínculo entre las actividades viscerales como las funciones respiratorias, cardiovasculares y gastrointestinales, y los estados de sueño-vigilia. El núcleo del tracto solitario no se proyecta directamente a la corteza cerebral (Saper, 1995), aunque sí se proyecta en varias áreas del tronco encefálico, talámico e hipotalámico que inervan la corteza y pueden mediar en EEG y respuestas del sueño, como el hipotálamo lateral, y núcleos del tálamo de la línea media.
Resumen
Aquí se discuten las principales regiones cerebrales que trabajan juntas para producir sueño y vigilia. Las neuronas del RAS juegan un papel en la excitación y el sueño hasta cierto punto. La “red ejecutiva” parece desempeñar un papel importante en la regulación de la capacidad de respuesta de la corteza a la estimulación externa. El hipotálamo anterior y pineal regulan y afinan muchas de estas funciones también.
Referencias
- Gallopin, T., Fort, P., Eggermann, E., Cauli, B., Luppi, P. H., Rossier, J., Audinat, E., Mühlethaler, M., & Serafin, M. (2000). Identificación in vitro de neuronas promotoras del sueño. Naturaleza, 404, 992—995.
- Hastings, M.H., Maywood, E.S., & Brancaccio, M. (2018). Generación de ritmos circadianos en el núcleo supraquiasmático. Nat Rev Neurosci. 19 (8), 453-469.
- Iwańczuk, W., & Guźniczak, P. (2015). Fundamentos neurofisiológicos de los fenómenos de sueño, excitación, conciencia y conciencia. Parte 1. Anestesiol Intensivo Ther. 47 (2), 162—167. doi:10.5603/AIT.2015.0015
- McGinty, D., y Szymusiak, R. (2000). El interruptor de sueño-vigilia: un despertador neuronal. Nat. Med. 6, 510—511.
- Reinoso-Suárez, F., de la Roza, C., Rodrigo-Angulo, M. L., de Andrés, I., Núñez, A., y Garzón, M. (2010). “Mecanismos gabaérgicos en el tegmento pontino oral ventral —el sitio de inducción del sueño REM- en la modulación de estados sueño-vigilia”, en GABA y Sleep, ed. J. M. Monti, S. R. Pandi-Perumal, y H. Möhler (Basilea: Birkhauser-Verlag), 233—252.
- Saper, C. B. (1995). “Sistema autónomo central”, en The Rat Nervious System, ed. G. Paxinos (San Diego: Prensa Académica), 107—135.
- Saper, C. B., Chou, T. C., y Scammell, T. E. (2001). El interruptor de sueño: control hipotalámico del sueño y la vigilia. Tendencias Neurosci. 24, 726—731.
Atribución
- Las estructuras cerebrales que te despiertan y te ponen a dormir de Bruno Dubuc bajo licencia Copyleft.
- Anatomía Funcional del Sueño No REM por Isabel de Andrés, Miguel Garzón y Fernando Reinoso-Suárez en Fronteras Neurociencia licenciada CC-BY 4.0
- La información sobre el sueño por NIH es de dominio público
- La Glándula Pineal por Libretextos no tiene licencia indicada.
- Neuroanatomía, Núcleo Supraquiasmático por Melinda A. Ma y Elizabeth H. Morrison con licencia CC-BY 4.0