17.3: Difosfato de tiamina (Vitamina B1)
- Page ID
- 72318
El difosfato de tiamina (\(ThDP\)a veces también abreviado\(TPP\) o\(ThPP\)) es una coenzima que, al igual que la PLP, actúa como un sumidero de electrones para estabilizar los intermediarios carbaniones clave. La parte más importante de la\(ThDP\) molécula desde un punto de vista catalítico es su anillo de tiazol.
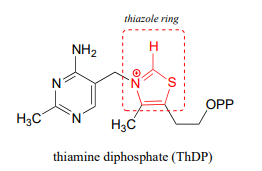
El protón en el carbono entre nitrógeno y azufre en el anillo de tiazol es débilmente ácido, con un\(pK_a\) of about 18.
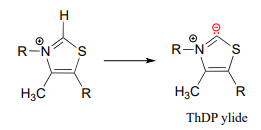
The reason for its acidity lies partly in the ability of the neighboring sulfur atom to accept, in its open \(d\)-orbitals, some of the excess electron density of the conjugate base. Another reason is that the positive charge on the nitrogen helps to stabilize the negative charge on the conjugate base. The deprotonated thiazole is called an ylide, which is a general term for a species with adjacent positively and negatively charged atoms.
The negatively charged carbon on the ylide form of \(ThDP\) is nucleophilic, and as we shall soon see, the first step of most \(TPP\)-dependent reactions is nucleophilic attack of the ylide carbon on a carbonyl group of the reaction substrate.
\(ThDP\) plays a key role in a variety of reaction types, but the common theme in all \(ThDP\)-dependent reactions is cleavage of a bond adjacent to the carbonyl carbon of a ketone or aldehyde.
Thiamine diphosphate assists in breaking bonds next to a ketone or aldehyde:
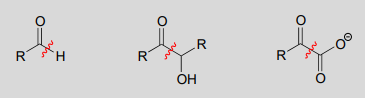
Consider this hypothetical decarboxylation step:
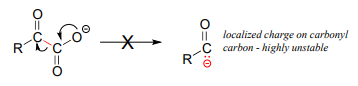
Esperemos que pueda reconocer rápidamente que este no es un paso químicamente razonable, porque la especie intermedia que resulta de la descarboxilación tiene una carga negativa localizada en el carbono de la cetona, un intermedio muy inestable e improbable de hecho.
(Recordemos de la sección 13.1 que las etapas de descarboxilación suelen dar como resultado intermedios en los que la carga formal negativa se deslocaliza en oxígeno o nitrógeno, es decir, enolatos o enaminas).
Ahora considere, sin embargo, una reacción que está ocurriendo en sus células en este momento, catalizada por la enzima piruvato descarboxilasa (EC 4.1.1.1):
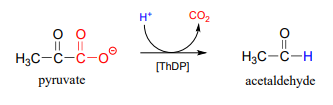
De alguna manera, la enzima logra lograr esta descarboxilación 'imposible'. ¿Cómo sucede esto? Aquí es donde entra en juego la coenzima tiamina difosfato.
A\(ThDP\)-dependent decarboxylation reaction (pyruvate decarboxylase):
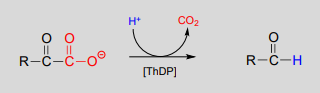
Mechanism:
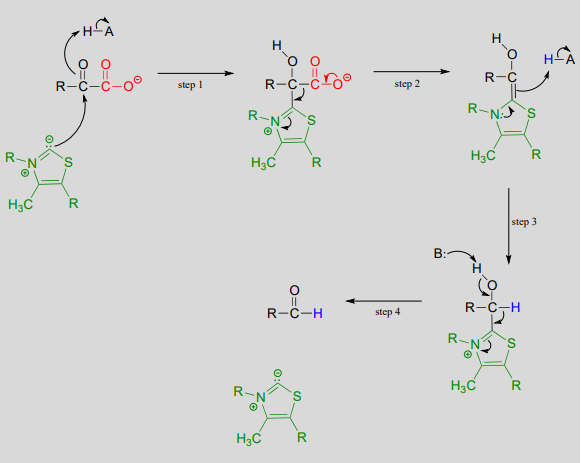
Upon binding to the enzyme's active site, \(ThDP\) quickly loses a proton. The nucleophilic ylide carbon then adds to the carbonyl carbon of pyruvate.
Look carefully at the intermediate that results from step 1 in the mechanism above. The thiazole ring of \(ThDP\), once it has added to the carbonyl of pyruvate, provides an 'electron sink' to absorb the electrons from decarboxylation (step 2). Note which bond is breaking in step 2 - as was mentioned earlier, the common function of \(ThDP\) is to make possible the cleavage of a bond to a carbonyl carbon.
In step 3, the electrons from decarboxylation flow back to abstract a proton from an acidic group in the active site. All that remains is for the product to break free of thiamine in step 4.
Thiamine can also assist in decarboxylation-addition reactions:
\(ThDP\)-dependent decarboxylation-addition:
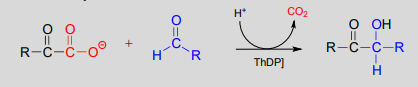
Mechanism:
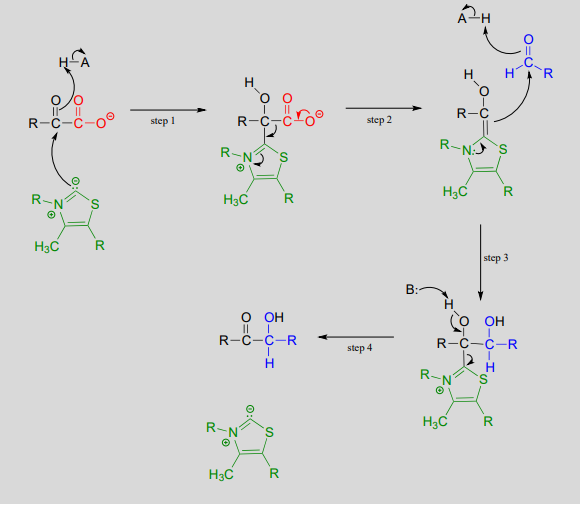
Here, the electron-rich intermediate formed from the decarboxylation step (step 2) simply goes on to act as a nucleophile rather than as a base, adding to the carbonyl group of an aldehyde or ketone (step 3). As before, the product breaks free of \(ThDP\) in step 4.
An example is the first step in the biosynthetic pathway for isoprenoid compounds in bacteria:

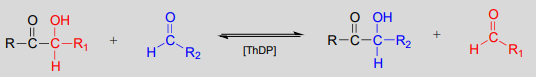
La transcetolasa, una enzima\(ThDP\) dependiente en la vía de pentosa fosfato del metabolismo del azúcar, cataliza una etapa de ruptura del enlace carbono-carbono, seguida de una etapa de formación de enlaces carbono-carbono. Los sustratos y productos se encuentran en niveles de energía similares, por lo que la reacción es completamente reversible.
Reacción de transcetolasa:
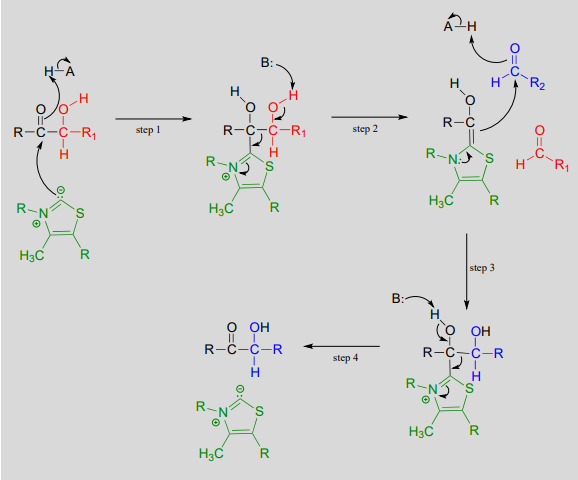
Mecanismo:
A continuación se muestra un ejemplo real de una transformación catalizada por transcetolasa a partir de la ruta de pentosa fosfato (mostrada en las proyecciones de Fischer, como es común para las estructuras de azúcar).
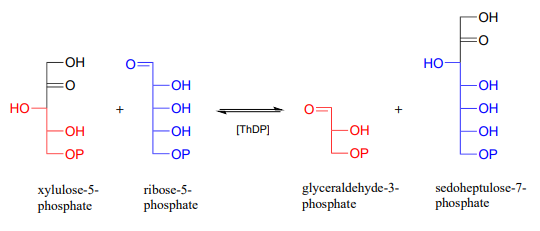
Como se mencionó anteriormente, la reacción de transcetolasa es altamente reversible. ¿Cree que lo mismo puede decirse de las reacciones de descarboxilación y descarboxilación-adición que vimos en esta sección? ¿Por qué o por qué no?
(¡Desafiante!) Proponer un mecanismo para la reacción a continuación.
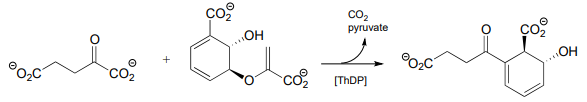
- Sugerencia
-
Se trata\(ThDP\) de una adición de descarboxilación/Michael facilitada, seguida de\(E1cb\) la eliminación del piruvato. Una adición de Michael es el nombre de una adición conjugada con un nucleófilo de carbono. (J. Mol. Biol. 2010, 401, 253).
Proponer un mecanismo para la reacción a continuación.
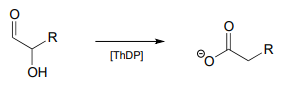
- Sugerencia
-
El mecanismo puede describirse como un paso\(ThDP\) de deshidratación facilitado, seguido de un paso de tautomerización, seguido de una expulsión hidrolítica de\(ThDP\) (un tipo diferente de\(ThDP\) expulsión de lo que han visto hasta ahora!)


