PLAN
- Définition et étiologie des leucorrhées
- Infections génitales basses (IGB)
- Mycose vaginale
- Vaginose bactérienne
- Vulvo-vaginite à Trichomonas vaginalis
- Vaginites bactériennes spécifiques
- Infections génitale hautes (IGH)
- Endocervicites
- Endocervicite à Neisseria gonorrhoeae
- Endocervicite à Chlamydia trachomatis
- cEndocervicite à Mycoplasma genitalium
- Infections utéro-annexielles (endométrites et salpingites)
Les infections génitales féminines sont nombreuses et variées. Elles sont causées par des microorganismes exogènes sexuellement transmissibles mais aussi par des germes issus de la flore vaginale commensale qui prolifèrent anormalement.
On distingue :
- les infections génitales basses (IGB) qui affectent le vagin, l’exocol et la vulve ;
- les infections génitales hautes (IGH) qui concernent l’endocol utérin, l’endomètre et les trompes utérines.
Définition et étiologies des leucorrhées
Les leucorrhées (ou pertes blanches) sont des écoulements non sanglants provenant de l’appareil génital. Leur observation constitue le symptôme majeur d’une infection génitale. Une leucorrhée n’est cependant pas toujours d’origine infectieuse.
On observe en effet :
- des leucorrhées physiologiques : Elles peuvent apparaître ponctuellement avant l’ovulation ou avant les règles et concrétisent l’accentuation passagère d’un phénomène physiologique : hyperdesquamation des cellules superficielles du vagin, hypersécrétion de glaire cervicale. Sous l’influence des œstrogènes, la sécrétion de la glaire cervicale augmente à partir du 10éme jour du cycle et atteint son maximum à l’ovulation. En cas d’abondance, cette sécrétion s’écoule à l’extérieur sous forme de pertes blanches. C’est le cas en particulier des états d’hyperœstrogénémie qui accompagnent assez souvent la puberté et la ménopause. La leucorrhée physiologique n’est jamais nauséabonde et n’entraîne jamais de signes cliniques tels que douleurs, irritation ou prurit.
- des leucorrhées d’origine endocrinienne : Elles sont observées lors de néoplasie (cancer) cervico-vaginale. Elles persistent quelle que soit la phase du cycle. Une leucorrhée de ce type est pathologique mais non infectieuse.
Dans les cas de leucorrhées physiologiques ou d’origine endocrinienne, la muqueuse vaginale apparaît saine ou atrophiée.
- des leucorrhées d’origine infectieuse : La muqueuse apparaît alors congestionnée et suppurée (vaginite) ou non suppurée (vaginoses ou mycoses vaginales). Les pertes sont abondantes, quelquefois malodorantes et persistantes en l’absence de traitement.
| Le rôle du laboratoire de microbiologie est de déterminer si les leucorrhées sont le signe d’une infection ou relève d’une autre étiologie. |
Infections génitales basses (IGB)
Quatre pathologies infectieuses affectent l’appareil génital bas de la femme :
- la mycose vaginale,
- la vaginose bactérienne,
- la vulvo-vaginite à Trichomonas vaginalis
- les vaginites bactériennes spécifiques.
Mycose vaginale
Les signes cliniques les plus courants sont : prurit, brûlures en fin de miction, dyspareunie (douleur ressentie lors des rapports sexuels).
Il ne s’agit pas d’une IST (infection sexuellement transmissible) mais d’un déséquilibre de la flore vaginale avec prolifération d’une levure commensale. En effet 15 à 20 % des femmes sont porteuses naturellement au niveau du vagin de Candida albicans. Sa prolifération, c’est-à-dire son passage à l’état pathogène, serait conditionnée par l’apparition de circonstances favorisantes qui, pour certaines, modifient le pH vaginal. Ces facteurs liés à l’hôte peuvent être séparés en :
- facteurs locaux : la contraception par les œstroprogestatifs, l’hygiène excessive et inadaptée comme l’abus de savons acidifiants, les vêtements serrés et synthétiques qui favorisent la macération et augmentent l’acidité locale, l’exposition fréquente à l’eau de piscine ou de mer.
- facteurs généraux : la grossesse, les antibiotiques à large spectre, le diabète, la corticothérapie, la chimiothérapie anticancéreuse, les immunosuppresseurs après transplantation d’organes.
Les levures en cause sont : Candida albicans (85 à 90% des cas), C. glabrata (femme enceinte), C. tropicalis et plus rarement C. balanitis.
L’examen gynécologique montre un érythème vulvaire et vaginal ainsi que la présence d’un enduit vaginal blanchâtre. Les sécrétions sont blanches, grumeleuses et inodores. Le pH est normal donc acide (pH< 4,5). L’apparition de ces signes cliniques après une antibiothérapie oriente vers une mycose.
Les symptômes d’allergie (prurit) s’expliquent par la libération de grandes quantités de candidine, une protéine allergisante.
Il n’y a pas de réponse inflammatoire de l’hôte (l’examen microscopique du frottis vaginal montre généralement peu de leucocytes).
Le traitement à base d’antifongique est local (ovule ou crème). Les rechutes sont fréquentes mais les causes restent souvent inconnues.
Vaginose bactérienne
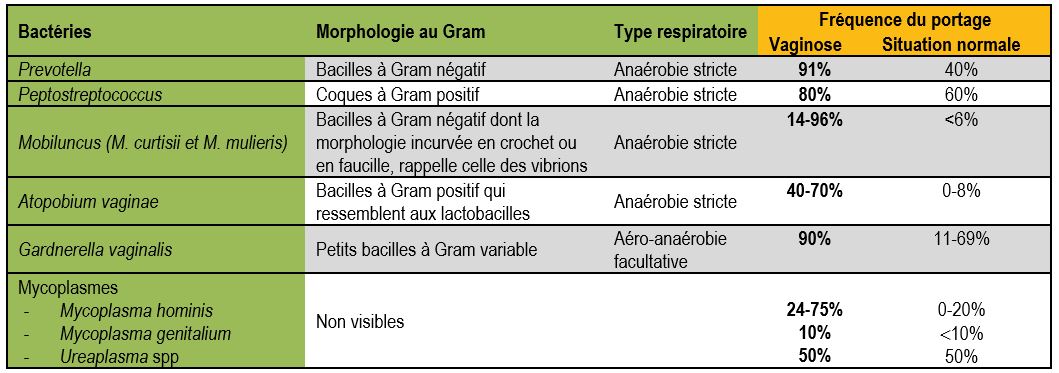
C’est la pathologie vaginale la plus fréquente. Tout comme la mycose, ce n’est pas une IST mais un trouble de l’écologie microbienne du vagin qui entraîne une prolifération polymicrobienne de bactéries de la flore commensale (100 à 100 000 fois la concentration normale) et une diminution importante des lactobacilles qui protègent normalement le vagin. Les bactéries en cause sont essentiellement des anaérobies stricts (surtout Prevotella spp., Peptostreptococcus, Mobiluncus, Atopobium vaginae), mais aussi Gardnerella vaginalis, Mycoplasma hominis : leur quantité et leur diversité sont fortement augmentées en cas de vaginose (voir tableau 2). D’après une étude récente Gardnerella vaginalis serait l’espèce la plus virulente.
Tableau 2 : les bactéries responsables de vaginose : comparaison de la fréquence du portage lors de vaginose et en situation normale
La moitié des patientes ne présentent pas de symptômes. S’ils existent, les principaux symptômes sont des leucorrhées abondantes, homogènes, grisâtres, adhérentes et malodorantes (odeur de poisson avarié liée aux amines).
Les amines (putrescine, cadavérine, méthylamine, 2-méthyl-propanamine, triméthylamine) produites par certaines bactéries anaérobies sont responsables d’une augmentation du pH (pH>4,5) et en partie de la symptomatologie allergique observée (hyperdesquamation de la muqueuse, œdème, prurit).
Les vaginoses bactériennes sont traitées avec du métronidazole (antibiotique actif sur les bactéries anaérobies strictes).
La vaginose bactérienne est une pathologie bénigne hors grossesse, mais représente une cause majeure de complications obstétricales dont l’accouchement prématuré. C’est pourquoi la HAS (Haute Autorité de Santé) recommande depuis 2001 de dépister systématiquement toutes les femmes enceintes à haut risque (ayant un antécédent de prématurité) en début de grossesse afin de les traiter.
Les amines (putrescine, cadavérine, méthylamine, 2-méthyl-propanamine, triméthylamine) produites par certaines bactéries anaérobies sont responsables d’une augmentation du pH (pH>4,5) et en partie de la symptomatologie allergique observée (hyperdesquamation de la muqueuse, œdème, prurit).
La moitié des patientes ne présentent pas de symptômes. S’ils existent, les principaux symptômes sont des leucorrhées abondantes, homogènes, grisâtres, adhérentes et malodorantes (odeur de poisson avarié liée aux amines)
On traite les vaginoses bactériennes avec du métronidazole (antibiotique actif sur les bactéries anaérobies strictes).
Vulvo-vaginite à Trichomonas vaginalis
C’est une IST due à un protozoaire flagellé, Trichomonas vaginalis. C’est le seul pathogène vaginal capable d’entrainer une inflammation de la muqueuse vaginale chez la femme pubère non ménopausée.
Après une incubation de 4 à 28 jours la vaginite à Trichomonas se manifeste essentiellement par trois symptômes : la leucorrhée, les brûlures, et les prurits vulvaires. La leucorrhée a un aspect caractéristique : elle est verdâtre, mousseuse, fluide, et d’abondance parfois considérable, légèrement nauséabonde (plâtre frais).
Le frottis est inflammatoire (nombreux granulocytes et quasi disparition des cellules vaginales). Les lactobacilles sont très souvent remplacés par une flore très souvent monomorphe composée d’un entérocoque, d’une entérobactérie ou de S. agalactiae. Les granulocytes sont très nombreux.
La patiente et tous les partenaires, puisqu’il s’agit d’une IST, seront traités au métronidazole.
Vaginites bactériennes spécifiques
Ces vaginites sont essentiellement retrouvées chez la petite fille ou la femme ménopausée. L’infection est toujours monomicrobienne : une bactérie provenant soit du groupe II ou soit du groupe III de la flore commensale (voir tableau 1) se multiplie abondamment au dépend des lactobacilles (groupe I) et entrainent une inflammation de la muqueuse vaginale (afflux de granulocytes neutrophiles). Les bactéries les plus fréquemment en cause sont : S. agalactiae (streptocoque B), E. coli ou S. aureus. Sont plus rarement rencontrées : Haemophilus influenzae, le pneumocoque, les entérocoques, les Neisseria et Moraxella.
Les raisons qui expliquent cette prolifération sont : l’immaturité de la muqueuse vaginale chez la fillette, des traitements antibiotiques ou hormonaux, des troubles trophiques vulvaires (sécheresse vaginale, atrophie vulvo-vaginale..) liés à une carence hormonale (comme au cours de la ménopause) mais aussi des facteurs liés à la bactérie elle-même.
Infections génitales hautes (IGH)
Contrairement au vagin, la cavité utérine et les trompes utérines sont naturellement stériles.
Les IGH sont le plus souvent des IST au cours desquels les germes progressent par voie ascendante et infectent l’endocol utérin (endocervicite), puis l’endomètre (endométrite) et enfin les trompes utérines (salpingite). Les salpingites peuvent s’accompagner d’une obstruction des trompes avec comme conséquence la stérilité (obstruction totale) ou un risque de grossesse extra utérine (obstruction partielle). Enfin les germes peuvent continuer leur progression dans les trompes utérines jusqu’au pavillon ; ce dernier s’ouvrant sur le péritoine, les IGH peuvent se compliquer de péritonite.
Les endométrites et salpingites sont aussi dénommées infections utéro-annexielles.
Endocervicites
La glaire cervicale représente un obstacle majeur à la progression ascendante des germes présents dans le vagin, d’où l’appellation verrou microbiologique.
Les agents responsables d’endocervicites présentent des facteurs de virulence spécifiques qui leur permettent de franchir ce « verrou microbiologique » et d’infecter les cryptes glandulaires. Ce sont les Neisseria gonorrhoeae et Chlamydia trachomatis (sérovars D, Da, E, F, G, H, I, IA, J et K). Ils infectent seuls ou ensemble l’endocol utérin. Ils sont introduits à ce niveau lors de relations sexuelles. Les endocervicites sont donc des IST.
Ces infections sont souvent asymptomatiques. Un écoulement cervical purulent, un col inflammatoire ou saignant, des signes d’infection urinaire et/ou une leucocyturie amicrobienne permettent d’évoquer une endocervicite à une de ces deux espèces. Une urétrite est fréquemment associée (le diagnostic des urétrites est présenté dans le chapitre sur les prélèvements génitaux chez l’homme).
Endocervicites à Neisseria gonorrhoeae (gonocoque)
L’infection gonococcique (après une incubation de 8 à 10 jours) passe le plus souvent inaperçue : les femmes n’ont pas de symptômes dans plus de 50% des cas. Lorsqu’elle est symptomatique, l’infection entraine des leucorrhées plus ou moins purulentes voire sanglantes et parfois des douleurs abdominales. Une urétrite accompagne très souvent l’endocervicite. En absence de traitement, l’infection peut progresser en direction de l’endomètre et surtout des trompes utérines(infections utéro-annexielles).
Chez la femme enceinte, une gonococcie non traitée peut provoquer un accouchement prématuré, une rupture prématurée des membranes, une conjonctivite chez le nouveau-né (risque de cécité).
Endocervicites à Chlamydia trachomatis (sérotypes D A K)
Chlamydia trachomatis est, en France, le microorganisme le plus fréquemment responsable d’IST. Comme le gonocoque il n’est pas capable d’infecter le vagin et n’entraine pas ou peu de symptômes chez la femme ce qui explique les complications sévères qui peuvent s’en suivre : endométrite, salpingite, stérilité et grossesse extra-utérine. L’infection est souvent découverte fortuitement à l’occasion d’un bilan d’hypofertilité.
Endocervicites à Mycoplasma genitalium
Mycoplasma genitalium est une très petite bactérie sans paroi, comme toutes les bactéries de la classe des Mollicutes, découverte en 1980. Elle fait partie des mycoplasmes génitaux avec Mycoplasma hominis et Ureaplasma spp. C’est la seule espèce de ce groupe à être responsable d’endocervicites (son pouvoir pathogène est certain). C’est une IST cosmopolite.
Le traitement antibiotique de choix est l’azithromycine, substitué par une fluoroquinolone en cas de résistance à ce macrolide.
Infections utéro-annexielles (endométrites et salpingites)
Les formes pauci- ou asymptomatiques sont habituelles ce qui explique la fréquence des séquelles : stérilité tubaire et grossesse extra-utérine. Quand elles sont symptomatiques, elles se manifestent par des douleurs pelviennes d’intensité variable, des leucorrhées et quelquefois par de la fièvre.
Ce sont le plus souvent des complications d’endocervicite. Les espèces isolées sont alors Neisseria gonorrhoeae, Chlamydia trachomatis ou Mycoplasma genitalium.
Certaines s’expliquent par une déficience du verrou microbiologique liées à un acte médical (pose de stérilet, hystéroscopie, curetage) ou une pathologie sous-jacente (polypes au niveau du col, cancer ou atrophie de l’endomètre,..).
Les espèces isolées appartiennent alors au groupe II et III de la flore vaginale comme les autres mycoplasmes urogénitaux (Mycoplasma hominis et Ureaplasma spp.)