Le remdésivir est l’un des médicaments les plus fréquemment prescrits aux patients hospitalisés en raison de la COVID-19.
Nous avons associé la bradycardie sinusale avec le remdésivir dans le traitement de ces patients.
Une association entre le remdésivir et la bradycardie est particulièrement pertinente pour plusieurs patients hospitalisés en raison de la COVID-19 qui présentent d’autres facteurs de risque de la bradycardie, comme un âge avancé, une maladie cardiovasculaire et la prise concomitante de bêtabloquants.
Un homme de 59 ans s’est présenté à l’hôpital avec une toux et un essoufflement après avoir obtenu un résultat positif à un test d’amplification en chaîne par polymérase du SRAS-CoV-2 une semaine auparavant. Il n’avait pas d’antécédents médicaux, son indice de masse corporelle était normal et il ne prenait pas de médicaments d’ordonnance ni en vente libre. Il ne fumait pas; il ne consommait pas de boissons alcoolisées ni de drogues à usage récréatif. Il demeurait dans une résidence multigénérationnelle et travaillait comme bijoutier.
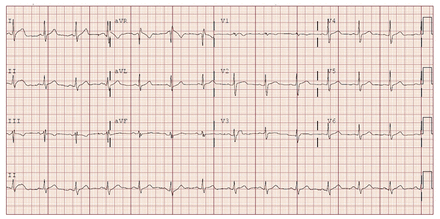
D’après son examen physique, ses signes vitaux étaient normaux (tension artérielle de 129/74 mm Hg, fréquence cardiaque de 89 battements/minute, température corporelle de 36,9 °C), mis à part une hypoxie nécessitant l’administration de 2 L d’oxygène par canule nasale. Il n’était pas en état de détresse respiratoire et ses examens cardiovasculaire, respiratoire et abdominal étaient normaux. Les résultats des examens de laboratoire de routine montraient une diminution de la numération lymphocytaire (1,1 × 109/L) et un niveau élevé de la protéine C-réactive (70 mg/L). La numération plaquettaire et les niveaux d’hémoglobine, de créatine, de troponine à haute sensibilité et d’enzymes hépatiques (alanine aminotransférase [ALT]) étaient normaux. Son électrocardiogramme (ECG) montrait un rythme sinusal normal avec une fréquence cardiaque de 79 battements/minute (figure 1) et sa radiographie thoracique montrait une silhouette cardiaque normale et une opacification modérée de la zone pulmonaire bilatérale moyenne à inférieure, concordant avec la COVID-19.
Électrocardiogramme d’un homme de 59 ans avant le traitement au remdésivir, montrant un rythme sinusal normal.
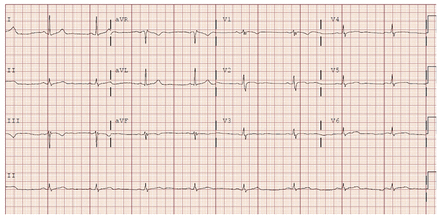
Le patient a été hospitalisé et nous avons amorcé un traitement de 6 mg de dexaméthasone quotidiennement et 40 mg d’énoxaparine injectée sous-cutanée tous les jours pour la prophylaxie de la thrombose veineuse profonde. Nous avons recruté le patient pour l’essai Solidarity de l’Organisation mondiale de la santé (OMS)1, l’essai randomisé ouvert de plasma de convalescent pour les adultes hospitalisés avec la COVID-19 présentant une atteinte respiratoire (CONCOR-1) et l’essai de décubitus ventral pour les patients atteints de la COVID-19 hospitalisés en médecine générale (COVI-PRONE); nous l’avons assigné aléatoirement au remdésivir, au plasma de convalescent et au décubitus ventral. Nous avons amorcé ces interventions au deuxième jour de son hospitalisation. Nous avons administré du plasma de convalescent la deuxième journée puis une première dose de 200 mg de remdésivir sous forme intraveineuse (IV), suivie de 100 mg de remdésivir IV la troisième journée et tous les jours par la suite. Le quatrième jour de son hospitalisation (c.-à-d., après sa troisième dose de remdésivir), il a développé une bradycardie sinusale accompagnée d’une fréquence cardiaque de 50 battements/minute (confirmée à l’ECG, figure 2). Il présentait une faiblesse généralisée, de la fatigue et des maux de tête, mais ne ressentait pas d’étourdissements ni de perte de conscience. Il n’avait pas de constipation, de nausées ni de douleur et aucun symptôme évoquant une augmentation du tonus vagal. Son analyse sanguine était notable en raison d’une élévation de l’alanine aminotransférase (ALT; 127 unités/L, limite supérieure de la normale 40) ainsi que des électrolytes (sodium, potassium, bicarbonate, calcium, magnésium, phosphate), de la thyréostimuline et des protéines C-réactives normaux. Nous avons retardé la quatrième dose de remdésivir en raison de sa bradycardie et de son ALT élevée. Après avoir interrompu le traitement au remdésivir, la fréquence cardiaque du patient a commencé à augmenter et au septième jour, elle atteignait 62 battements/minute, son ALT était de 133 unités/L et il a obtenu son congé (figure 3). Nous n’avons pas repris le traitement au remdésivir.
Électrocardiogramme après 3 doses du traitement au remdésivir, montrant une bradycardie sinusale.
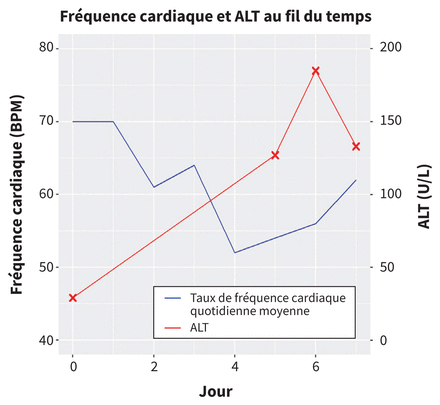
Variations de la fréquence cardiaque quotidienne moyenne (battements par minute [BPM]) et de l’alanine aminotransférase (ALT; unités/L) de la première journée d’hospitalisation au moment du congé. Nous avons amorcé le traitement au remdésivir au jour 2 et l’avons interrompu au jour 5.
Discussion
Nous avons obtenu l’approbation de la Federal Drug Administration (FDA) des États-Unis pour utilisation d’urgence du remdésivir dans le cadre du traitement de patients atteints de la COVID-19 nécessitant une hospitalisation2. Santé Canada a approuvé le remdésivir pour les patients hospitalisés en raison d’une forme grave de la COVID-19 accompagnée d’une pneumonie et requérant une oxygénothérapie3.
Les 2 plus grands essais cliniques randomisés et contrôlés (ERC) évaluant l’efficacité et l’innocuité du remdésivir sont l’Adaptive COVID-19 Treatment Trial (ACTT-1) et l’essai Solidarity, organisé par l’Organisation mondiale de la santé1,4. L’ACTT-1 a révélé que les patients assignés aléatoirement au remdésivir (n = 541) se rétablissaient plus rapidement que les patients assignés aléatoirement au placebo (c.-à-d., 15 jours c. 10 jours, p < 0,001)4. L’essai Solidarity a démontré que les patients assignés aléatoirement au remdésivir (n = 2750) présentaient un taux de mortalité semblable aux patients assignés aléatoirement à la norme thérapeutique1. Malgré l’absence de données probantes démontrant une diminution de la mortalité dans l’essai Solidarity, le remdésivir est l’un des médicaments les plus communément prescrits aux patients hospitalisés en raison de la COVID-19. On estime que plus de 2 millions de doses de remdésivir ont été administrées à l’échelle mondiale pendant la pandémie de COVID-196.
Le remdésivir est un promédicament intraveineux issu d’un analogue de l’adénosine conçu à l’origine dans le cadre de programmes de recherche sur l’hépatite C et le virus respiratoire syncytial et plus tard modifié pour le traitement de l’Ebola. Il inhibe la polymérase de l’acide ribonucléique (ARN) viral et son action est efficace contre une large gamme de virus, dont le coronavirus du syndrome respiratoire du Moyen-Orient, le SRAS et le SRAS-CoV-24. Ce promédicament est généralement bien toléré bien que la transaminite, qui se manifeste principalement par des ALT élevées, en soit un effet indésirable fréquemment observé chez les patients et les participants sains à qui on administre le remdésivir2.
De récentes études de cas signalent que le remdésivir pourrait aussi causer la bradycardie5,7,8. Notre patient présentait à la fois des ALT élevées et une bradycardie sinusale. Bien qu’il n’y ait aucune conséquence clinique négative à cette dernière, si le remdésivir cause bien la bradycardie, ce point sera particulièrement pertinent pour les patients hospitalisés en raison de la COVID-19 qui présentent d’autres facteurs de risque de la bradycardie (p. ex., un âge avancé, la prise concomitante de bêtabloquants). Notre discussion portera principalement sur les associations potentielles entre le remdésivir et la bradycardie et résumera sommairement les données d’efficacité et d’innocuité du remdésivir.
Les événements indésirables fréquemment relevés avec le remdésivir (incidence de 1 %–10 %) comprennent des éruptions cutanées, des maux de tête, des nausées, de la diarrhée et une élévation modérée à grave des transaminases2,4. Bien que rares, des réactions d’hypersensibilité (anaphylactiques ou liées à la perfusion), de l’hypotension et de l’insuffisance rénale peuvent aussi se produire (incidence < 0,1 %). Dans l’essai ACTT-1, des arythmies (autres que la fibrillation ventriculaire et la tachycardie, la tachycardie supraventriculaire et la fibrillation auriculaire) ont affecté 0,2 % des patients recevant le remdésivir, comparativement à aucun cas rapporté dans le groupe placebo. Des données spécifiques à la bradycardie n’ont pas été rapportées.
D’autres complications cardiaques potentielles observées avec le remdésivir comprennent de la tachycardie supraventriculaire, que l’on a rapportée chez 0,6 % des patients du groupe expérimental de l’essai ACTT-1 (comparativement à 0,4 % pour le groupe contrôle) et de la fibrillation auriculaire grave chez 0,9 % des patients du groupe expérimental (comparativement à 0,2 % pour le groupe contrôle). Un cas d’arrêt cardiaque est aussi survenu au cours d’un traitement au remdésivir chez 0,6 % des patients d’un essai clinique randomisé de remdésivir contre le placebo (comparativement à aucun incident dans le groupe contrôle)7. L’essai ACTT-1 rapporte des arrêts cardiaques chez 1,9 % des patients recevant le remdésivir comparativement à 1,4 % chez ceux recevant le placebo. De plus, dans le cadre de l’essai clinique initial évaluant le remdésivir pour le traitement de l’Ebola, 1 patient sur 175 présentait de l’hypotension menant à un arrêt cardiaque après avoir reçu le remdésivir, lequel a été considéré comme potentiellement relié au médicament7.
Bien que les essais ACTT-1 ou Solidarity n’aient pas relevé la bradycardie comme un effet indésirable potentiel, les essais cliniques sont généralement dotés d’une puissance statistique insuffisante pour détecter les événements indésirables peu fréquents9. Des études de cas récentes ont décrit 4 cas de bradycardie sinusale chez des patients atteints de la COVID-19 qui avaient reçu du remdésivir (tableau 1)5,7,8. Gubitosa et ses collègues ont décrit un cas où une femme de 54 ans présentant un bloc de branche gauche du faisceau de His de cause inconnue a développé une bradycardie sinusale marquée de 38 battements/minute dans les 24 heures suivant une première dose de remdésivir contre la COVID-19, accompagnée d’un léger élargissement du complexe QRS et un allongement de son intervalle QT (QTc à 496 ms à partir de 440 ms). Sa bradycardie s’est aggravée jusqu’à un nadir de 34 battements/minute après sa troisième dose et on a dû lui administrer temporairement de l’atropine afin de traiter une angine et de l’hypotension7. Sanchez-Codez et ses collègues ont décrit le cas d’un garçon de 13 ans présentant une bradycardie sinusale grave (fréquence cardiaque de 40 battements/minute), mais autrement en santé, après avoir reçu une troisième dose de remdésivir5. Sa bradycardie s’est résorbée dans les 24 heures après la cessation du traitement au remdésivir. Une bradycardie sinusale transitoire associée à un allongement de l’intervalle QT (QTc de 439 ms à 555 ms) a aussi été rapportée chez une femme de 26 ans présentant des antécédents médicaux d’obésité qui avait été traitée au remdésivir contre la COVID-19. Une femme de 77 ans présentait une bradycardie transitoire semblable après une administration de remdésivir8. De plus, la FDA a rapporté 9 cas de bradycardie associés à l’utilisation du remdésivir contre la COVID-19 entre les mois de janvier et juin 2020 qui n’étaient pas associés à une réaction liée à la perfusion10.
Rapports de bradycardie sinusale chez des patients atteints de la COVID-19 auxquels on administre du remdésivir
Il existe plusieurs mécanismes possibles pour expliquer les effets cardiaques indésirables observés avec le remdésivir. Tout d’abord, l’un des métabolites actifs du remdésivir est semblable à l’adénosine triphosphate, pour laquelle il est démontré qu’elle réduit l’automaticité du nœud sinoauriculaire par le biais de la stimulation vagale, laquelle cause la bradycardie sinusale11. Bien que le remdésivir présente une affinité de liaison marquée avec les polymérases virales, toute réactivité croisée avec l’ARN polymérase mitochondriale humaine pourrait mener à un dysfonctionnement mitochondrial, ce dernier étant un mécanisme connu de la cardiotoxicité médicamenteuse5,8. Des études in vitro de cardiomyocytes dérivés de cellules souches humaines traitées au remdésivir ont démontré une cytotoxicité médicamenteuse pour les myocytes cardiaques12. Choi et ses collègues ont révélé que les effets cytotoxiques du remdésivir sur les cardiomyocytes s’accroissent avec le temps, de telle sorte qu’un traitement d’une plus longue durée (48 heures contre 24 heures) était associé avec une viabilité cellulaire moindre12. De surcroît, étant un analogue de l’adénosine, le remdésivir pourrait altérer la conduction nodale auriculo-ventriculaire, laquelle pourrait expliquer l’allongement du complexe QRS observé dans les cas précédents5,7,8. Davantage d’études sont nécessaires pour mieux évaluer ces mécanismes et leurs effets, particulièrement sur l’activité du nœud sinoauriculaire.
Dans le cas de notre patient, la bradycardie s’est manifestée rapidement après l’administration du médicament (figure 3) et son état s’est amélioré dans les 48 heures suivant la cessation du traitement. Il ne prenait aucun autre médicament qui pourrait autrement expliquer la bradyarythmie observée et aucun paramètre clinique n’évoquait une élévation du tonus vagal. Bien que les études de cas ne puissent établir la causalité, ce décours temporel éveille des soupçons sur l’imputabilité du remdésivir. De plus, bien qu’on ait rapporté de la bradycardie parmi les patients atteints d’une forme grave de la COVID-19, notre patient ne présentait pas de bradycardie lors de son hospitalisation et celle-ci ne s’est manifestée qu’après l’administration du remdésivir alors que son état clinique s’améliorait7,10. Par ailleurs, notre patient avait un score de 6 sur l’échelle Naranjo de probabilité de réaction indésirable médicamenteuse, un score qui semble indiquer une association causale probable entre le remdésivir et la bradycardie13. Nous n’avons pas retenté la médication puisque le patient se portait suffisamment bien pour obtenir son congé.
Conclusion
Notre étude de cas contribue à la documentation concernant l’association entre le remdésivir et la bradycardie. Cette association est pertinente, car le remdésivir est l’un des médicaments les plus fréquemment prescrits pour le traitement des patients hospitalisés en raison de la COVID-19. Bien que notre patient n’a pas subi de conséquences cliniques graves, nos observations sont pertinentes pour les patients plus âgés ou ceux qui prennent des médicaments reconnus pour causer la bradycardie. Après tout, l’âge moyen des patients hospitalisés atteints de la COVID-19 est environ 70 ans et plusieurs présentent une maladie cardiovasculaire ou de l’hypertension et prennent des bêtabloquants2. Des données probantes provenant d’études de cohortes étendues sont nécessaires pour comprendre si notre étude de cas représente une fausse causalité ou une association réelle.
Footnotes
Voir la version anglaise de l’article ici: www.cmaj.ca/lookup/doi/10.1503/cmaj.210300
Intérêts concurrents: Michael Fralick est un co-investigateur de l’essai clinique Solidarity et il a obtenu des subventions des Instituts de recherche en santé du Canada pour soutenir son travail. Le Dr Fralick est aussi consultant pour une entreprise en démarrage située au Massachusetts Institute of Technology qui a élaboré un test diagnostique basé sur la technique CRISPR pour la maladie à coronavirus 2019. Husam Abdel-Qadir signale avoir reçu des honoraires personnels de la compagnie Amgen, indépendamment des travaux soumis, ainsi que des versements du Canadian Vigour Centre (un organisme de recherche universitaire) pour siéger au comité externe et indépendant de validation des critères d’évaluation de l’essai THEMIS qui était financé par AstraZeneca. Aucun autre intérêt concurrent n’a été déclaré.
Cet article a été révisé par des pairs.
Les auteurs ont obtenu le consentement du patient.
Collaborateurs: Leora Branfield Day et Michael Fralick ont contribué à l’élaboration et à la conception du travail et ils ont produit la première ébauche du manuscrit. Tous les auteurs ont révisé de façon critique son contenu intellectuel important, ont donné leur approbation finale pour la version destinée à être publiée et endossent l’entière responsabilité de tous les aspects du travail.
Il s’agit d’un article en libre accès distribué conformément aux modalités de la licence Creative Commons Attribution (CC BY-NC-ND 4.0), qui permet l’utilisation, la diffusion et la reproduction de tout médium à la condition que la publication originale soit adéquatement citée, que l’utilisation se fasse à des fins non commerciales (c.-à-d., recherche ou éducation) et qu’aucune modification ni adaptation n’y soit apportée. Voir: https://creativecommons.org/licenses/by-nc-nd/4.0/deed.fr