扩张性心肌病

许多扩张型心肌病患者没有症状或症状轻微。一些症状包括:
- 呼吸短促
- 脚踝、小腿和腹部肿胀
- 过度疲劳
- 头晕
- 昏厥
- 心悸
- 胸痛/胸闷
病例介绍(Case Presentation)
一名48岁的男子因最近几天呼吸困难加重(Worsening breathlessness)而来到急诊室。呼吸困难(Dyspnea)在晚上加重,他需要在头下垫两个或多个枕头才能入睡。然而,由于夜间呼吸困难,经常惊醒。在过去的4个月里,在步行和爬楼梯时,疲劳(Fatigue)逐渐加重。
患者没有糖尿病或高血压,否认有胸痛(Chest pain)、心悸(Palpitation)或晕厥(Syncope)。他不吸烟,但在过去的30年里,一周中多数时间都要喝5-6大杯酒(5-6 large pegs of alcohol,注:1 peg≈60 ml)。他的家人都没有心脏病病史。
经检查,他呼吸急促(Tachypneic),发汗(Diaphoretic)。脉搏急促而微弱(Feeble),交替搏动(Alternate beats)时容量变化(Changing volume),四肢冰冷(Cold extremities),心率为120次/分,血压为106/74mm Hg。JVP明显升高,脚踝也出现了凹陷性水肿(Pitting edema)。肝边缘在右肋缘下6cm(6 cm below the right costal margin)处可触及。
心尖搏动(Apex beat)弥散,并向腋窝移位(Displaces toward the axilla)。S1和S2正常,二尖瓣区可闻及柔和的全收缩期杂音(Pansystolic murmur),舒张期早期(Early diastole)有可听到奔马律(Gallop)。两肺野下三分之一(Lower one-third of both lung fields)处可闻及双侧基底罗音(Bilateral basilar rales)。
临床讨论(Clinical Discussion)
从病史和体格检查来看,这名患者明显患有充血性心力衰竭(Congestive cardiac failure)。心力衰竭本质上是收缩性的(Systolic in nature),属于低输出量类型(Of the low output variety),起源于双心室(Biventricular in origin)。
心电图显示窦性心动过速(Sinus tachycardia)、窄QRS波群(Narrow QRS complexes)和非特异性T波倒置(Non-specific T-wave inversion),无任何S-T段移位或Q波(Without any S-T segment shift or Q-waves)。
胸部X线表现为中度心脏肥大(Moderate cardiomegaly)、Kerley B线、肺门充血(Hilar congestion)和头向集中化血管(Cephalized vessels),伴有肺水肿(Pulmonary edema)和少量右侧胸腔积液(Pleural effusion)(图12.1)。

图12.1 X线显示左心室收缩功能不全的经典发现。
注:Cephalization of vessels:肺血管集头现象;Bronchial cuffing:支气管袖套征;Kerley B lines: Kerley B线;Hilar vasculature congestion:肺门血管充血;Cardiomegaly:心脏肥大
小编注:
Pulmonary cephalization:肺血管头向集中/肺血管集头现象。指的是血液重新分布到上叶血管中,当上叶静脉与下叶静脉直径相同或更大时,可以进行诊断,是肺静脉高压的表现。(当静水压力超过10 mm Hg,液体开始泄漏到肺间质中。液体压迫下叶血管,之后,上叶血管被募集以分配更多的血液,上叶血管的尺寸增大。)
Kerley B线:是由于肺间质水肿引起小叶间隔增宽,在两肺下野外侧可形成水平线状影,常位于肋膈角区,为长约1-3厘米、宽约1-2毫米的水平横线,一般垂直于侧肋胸膜,是肺小叶间隔内积液的表现。
ECHO显示左心室扩张(Dilated left ventricle),射血分数25-30%,间隔和后壁运动减少(普遍性运动功能减退,Global hypokinesia)。二尖瓣小叶的偏移减少(Reduced excursion),E峰间隔分离(E-point septal separation, EPSS)增加(图12.2)。无局部壁运动异常或心脏瓣膜结构异常。存在轻度二尖瓣反流(Mild mitral regurgitation)和轻度右心室扩张。

图 12.2 ECHO显示室间隔和二尖瓣叶减少偏移。
为了帮助大家更好的理解EPSS,给大家另配一张M型超声图(见下图)。
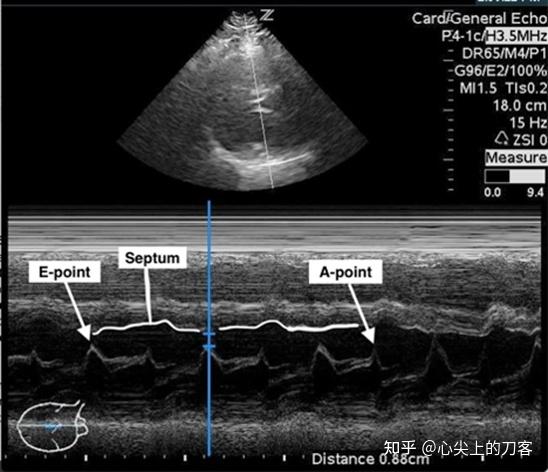
小编另配图:M型超声上的二尖瓣波形包含两个峰值。第一个较大的峰值称为“E点”,对应于左心室舒张早期的最大二尖瓣开口。第二个较小的峰值称为“A点”,对应于左心室舒张后期的心房收缩。
在正常功能的心脏中,二尖瓣应该打开,小叶撞击或在E点非常接近室间隔。因此,E点和室间隔之间的距离(EPSS)很小,这个距离称为E点间隔/E峰间隔分离(EPSS,E-point Septal Separation)。
因此,EPSS与LVEF呈负相关。EPSS>7 mm是LVEF降低的证据。EPSS≥ 13mm与左心室功能严重下降相关,对应估计LVEF为≤35%。在图中,EPSS为8.8 mm,表明收缩功能异常。
因此,本病例有三种主要的诊断可能性,包括:
- 器质性二尖瓣反流(Organic mitral regurgitation)
- 缺血性心肌病(Ischemic cardiomyopathy)
- 扩张型心肌病(Dilated cardiomyopathy)
在本病例中,二尖瓣结构正常(Normal in architecture),瓣膜反流的严重程度仅为轻度(Mild),因此不太可能是器质性二尖瓣反流(Organic mitral regurgitation)导致的严重左心室功能障碍(Severe left ventricular dysfunction)。
缺血性心肌病(Ischemic cardiomyopathy)是一种诊断可能性,但有几个反对这种诊断的原因。患者无明显的冠状动脉危险因素(Coronary risk factors)或心脏病家族史(Family history)。心电图未显示任何S-T段移位或Q波的存在。在ECHO上,显示普遍性运动机能减退(Global hypokinesia)而非局部壁运动异常(Not regional wall motion abnormality)。此外,左心室壁没有任何运动障碍节段(Dyskinetic segments),而存在右心室扩张(Right ventricular dilatation)(表12.1)。

RWMA (Regional wall motion abnormality):节段性室壁运动异常
因此,本病例最可能的诊断是扩张型心肌病(Dilated cardiomyopathy,DCMP)。扩张型心肌病(DCMP)有几种原因。
- 特发性变异(Idiopathic variety)被认为是在急性病毒性心肌炎之后出现的。
- DCMP的主要明确原因是重度酒精中毒(Heavy alcoholism)、糖尿病和围产期(Peri-partum)。
- 家族性DCMP见于杜氏肌营养不良症(Duchenne’s muscular dystrophy)和弗里德里希共济失调(Friedrich’s ataxia)。
- 缺乏硫胺素(Thiamine, 维生素B1)、硒(Selenium)和肉碱(Carnitine)可导致可逆形式的DCMP。
- 导致DCMP的药物有多柔比星(Doxorubicin)、伊马替尼(Imatinib)、环磷酰胺(Cyclophosphamide)和曲妥珠单抗(Trastuzumab)。
- 罕见的是,任何原因引起的持续性心动过速(Persistent tachycardia)均可导致永久性DCMP(表12.2)。

小编注:
- Duchenne’s muscular dystrophy:杜氏肌营养不良症(假性肥厚性营养不良症),是最常见的肌营养不良,为X连锁隐性遗传(由雌性携带,但只影响雄性)。
- Friedrich’s ataxia:弗里德里希共济失调,是一种常染色体隐性遗传疾病,会对神经系统造成进行性损害。表现为协调性差的初始症状,如步态障碍;也会导致脊柱侧弯、心脏病和糖尿病,但不会影响认知功能。
相关检查(Pertinent Investigations)
虽然超声心动图是扩张型心肌病(DCMP)的可靠诊断方式,但可以进行一系列测试来确定病因诊断。这是因为DCMP有多种原因,需要进行积极的研究以确定可治疗的原因,并乐观地预防疾病的无情发展。
炎症标志物(ESR和CRP)在心肌炎(Myocarditis)中升高,而生物标志物(CPK、LDH)在心肌坏死(Myocardial necrosis)中水平升高。对患者进行慢性感染(HIV、丙型肝炎)或营养缺乏(硫胺素、硒、肉碱)筛查。
注:CPK,肌酸磷酸激酶;LDH:乳酸脱氢酶。
如果怀疑贫血(Anemia)或血色素沉着病(Hemochromatosis),则需要检查血清铁(Serum iron)、铁蛋白(Ferritin)和转铁蛋白(Transferrin)。如果要排除甲状腺毒症(Thyrotoxicosis),则需要进行T3、T4和TSH检查。进行肾和肝功能测试以评估液体超负荷(Fluid overload)的其他原因。
心脏磁共振成像(MRI)有助于评估左心室大小和几何结构(Geometry)、左心室重塑(LV remodelling)以及钆增强(Gadolinium enhancement)的组织特征(Tissue characterization)。
冠状动脉造影是在存在动脉粥样硬化危险因素的情况下进行的。心肌内膜活检(Endomyocardial biopsy),由于其诊断率低,很少进行。
管理问题(Management Issues)
DCMP管理的第一步是识别和治疗可逆因素。
措施包括停用激惹药物(Offending drugs)和纠正任何营养缺陷(Nutritional deficiency)。戒酒(Abstinence from alcohol)和控制糖尿病同样重要。心动过速相关的扩张型心肌病(Tachycardia related cardiomyopathy)必须控制心率。
大多数这些患者的治疗都是按照标准的心力衰竭治疗进行的(On the lines of standard heart failure therapy)。利尿剂(Diuretics)用于治疗液体超负荷(Fluid overload),肾素-血管紧张素系统调节剂 (Modulators of renin-angiotensin system) (ACE抑制剂或ARB)用于减少心脏后负荷(Afterload)。
当出现极度心动过速(Extreme tachycardia)或心房颤动(Atrial fibrillation)时,使用β受体阻滞剂。如果患者患有持续性心房颤动(Persistent atrial fibrillation),则需要使用地高辛(Digoxin)控制心率。
此外,患者开始口服抗凝剂(Oral anticoagulant),以降低血栓栓塞并发症(Thrombo-embolic complications)的风险。
最近的进展(Recent Advances)
很大比例的扩张型心肌病患者死于(Succumb to)恶性室性心律失常(Malignant ventricular arrythmias),而不是心力衰竭本身(Heart failure per se)。
抗心律失常药物(Antiarrhythmic drugs)除了其全身副作用(Systemic side-effects)外,还可降低射血分数并具有致心律失常的潜力(Proarrhythmic potential)。现在提倡使用自动植入式心脏复律除颤器(Automatic implantable cardioverter defibrillators, AICD)作为此类患者心脏猝死(Sudden cardiac death, SCD)的主要预防策略。
抗凝治疗(Anticoagulant therapy)广泛适用于房颤患者和有附壁血栓(Mural thrombus)记录的患者。目前,正在进行试验,评估抗凝剂对窦性心律(Sinus rhythm)患者血栓栓塞并发症的作用。
对于中度至重度症状(NYHA III级或IV级)的严重左心室功能障碍(LVEF低于30%)和宽QRS波群(QRS持续时间超过120毫秒)的患者,可提供心脏再同步治疗(Cardiac resynchronization therapy, CRT)。
如果存在左束支传导阻滞(LBBB)或室内传导障碍(Intraventricular conduction defect, IVCD),则放置双心室起搏器(Biventricular pacemaker)以同步右心室和左心室的射血。
最后,可植入心室辅助装置(Ventricular assist device,VAD),以改善血流动力学严重恶化(Hemodynamic deterioration)患者的左心室功能。作为进行心脏移植之前(Cardiac transplantation)的桥接,这种策略特别有用。

(完)
